
题目列表(包括答案和解析)
(11分)1866年H. Rithausen从谷胶的硫酸分解产物中分离出谷氨酸(![]() )。1890年L. Wollf合成并确定了它的结构,1908年池田菊苗从海带的热水提取物中分离出谷氨酸的钠盐(
)。1890年L. Wollf合成并确定了它的结构,1908年池田菊苗从海带的热水提取物中分离出谷氨酸的钠盐(![]() ),它才是具有鲜味的成分,即味精。
),它才是具有鲜味的成分,即味精。
10-1 谷氨酸的电离常数Ka1=6.46×10-3,Ka2=5.62×10-5,Ka3=2.14×10-10;pKa= -lgKa,所以pKa1=2.19,pKa2 = 4.25,pKa3 = 9.67。
目前工业上生产味精的方法有水解法、糖蜜提取法、淀粉发酵法及合成法等。当前我国生产的味精主要采用淀粉发酵法。
以发酵法生产的工艺流程如下:淀粉![]() 葡萄糖
葡萄糖![]() 发酵
发酵![]() 谷氨酸铵
谷氨酸铵![]() L-谷氨酸
L-谷氨酸![]() 谷氨酸-钠盐。
谷氨酸-钠盐。
若生成谷氨酸二钠盐,则不具有鲜味,所以工业生产中控制各阶段的pH是一项关键。
(1)Ka1、Ka2、Ka3相对应的基团各是哪个?
(2)计算谷氨酸等电点的pH(所谓等电点,就是谷氨酸呈电中性时所处环境的pH)。在下面正确的选项上画圈。
A.2.19 B.3.22 C.4.25 D.6.96
(3)中和、脱色、结晶时的pH应保持在多少?在下面正确的选项上画圈。
A.3.22 B.4.25 C.6.96 D.9.67
(4)用什么物质脱色?
10-2 味精中有效成分是谷氨酸钠,可用沙伦逊甲醛滴定法测定其含量。准确称取味精1.000g,加蒸馏水溶解后稀释到10.0mL;从中取2.0mL放入100mL锥形瓶中,加入2.0mL 36%的甲醛溶液,加入20mL水。以酚酞为指示剂,用0.1000mol/L的标准NaOH溶液进行滴定,消耗10.80mL。
(1)谷氨酸钠与甲醛反应得到化学式为C6H8NO4Na,写出结构简式。
(2)加入甲醛的目的是什么?
10-3 味精中往往会加入食盐,某学生设计如下实验方案测定NaCl含量:取味精样品5.0g,并溶于蒸馏水;加入足量用稀硝酸酸化的硝酸银溶液,使沉淀完全;过滤;用蒸馏水反复洗涤沉淀多次;将沉淀低温烘干、称量;重复操作3次,计算NaCl含量。
另一学生觉得这个实验方案的误差较大,且测定沉淀的质量很不方便。于是他设计了另一个实验方案来测定NaCl的含量。已知AgSCN是难溶于水的沉淀。
请简要写出测定NaCl含量的新方案。


Fe(OH)2是铁的一种氢氧化物,难溶于水,具有还原性,其制备方法较为特殊。下面是实验室制备
Fe(OH)2的方法之一:
(1)制备原理:利用复分解反应,使可溶性的亚铁盐溶液与可溶性的碱液反应生成Fe(OH)2。写出该反应的离子方程式_________________。
(2)NaOH溶液的制备:在试管中加入2~3 mL蒸馏水,加热至沸腾,冷却至室温,加入1片NaOH固体。制备NaOH溶液的蒸馏水加热的目的是___________。
(3)FeSO4溶液的制备:在试管中加入5 mL蒸馏水,并加热,直至蒸馏水沸腾,然后向蒸馏水中滴入几滴稀硫酸;待蒸馏水冷却至室温,加入少量FeSO4晶体,为了防止溶液中的Fe2+被氧化,在溶液中加入少量
____________。加入FeSO4晶体前在蒸馏水中加入稀硫酸的目的是____________。
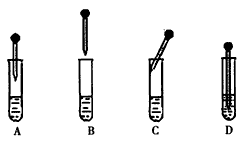
(4) Fe(OH)2的制备:下图中的胶头滴管中盛有NaOH溶液,试管中是FeSO4溶液。制备Fe(OH)2时正确的操作是___________(填字母序号),操作过程中________(填“能”或“不能”)振荡试管,原因是___________________。
已知KClO3溶液呈中性.Cl-与Ag+反应生成AgCl,每次新生成的AgCl中有10%(质量分数)见光分解成单质银和氯气,氯气可在水中歧化成HClO3(强酸)和HCl,HCl中的Cl-又与剩余的Ag+反应生成沉淀,如此循环往复,直至终了.
(1)写出上述各步反应的总化学方程式.
(2)现向含1 mol NaCl的溶液中加入足量的AgNO3溶液,问:最终能生成多少克难溶物(Ag和AgCl)?若最后所得溶液的体积为1.2 L,则溶液的H+浓度是多大?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com