
题目列表(包括答案和解析)
(08宁波市模拟)阅读下列两段材料,请回答下列问题:
材料一:2006年全国理综Ⅰ第9题:把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为()
A.1∶2∶3 B.3∶2∶1
C.6∶3∶1 D.6∶3∶2
材料二:己知下列表中有关物质的熔、沸点如下:
物质 | K2O | MgO | Al2O3 | KCl | MgCl2 | AlCl3 |
熔点(℃) | 881 | 2852 | 2050 | 711 | 714 | 190(259kPa) |
沸点(℃) | ― | 3600 | 2980 | 1437 | 1412 | 181 |
(1) 有人认为材料一中的题干与选项有矛盾。若选项正确,则结合材料二可推知氯化钾、氯化镁、氯化铝三种物质中有一种物质是不符合题意的,这种物质是 ,其理由是 。
(2) 有人认为材料一中的题干正确,只要把一个正确的选项补加进去就是一道好题,你认为选项改加:“(Ⅰ) 0∶0∶0”和“(11) 6∶3∶0”哪个好? (填写编号)
(3) 也有人认为只要把氯化钾、氯化镁、氯化铝中的其中一种物质改为材料二表格中另一种物质也符合题意。写出电解这种物质时刚极的电极反应方程式: 。
(4) 设计可靠实验证明:MgCl2、AlCl3所属的品体类型,其实验方法是 。
阅读下列两段材料,请回答下列问题:
材料一:2006年全国理综Ⅰ第9题:把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为________
A.1∶2∶3
B.3∶2∶1
C.6∶3∶1
D.6∶3∶2
材料二:已知下列表中有关物质的熔、沸点如下:

(1)有人认为材料一中的题干与选项有矛盾,若选项正确,则结合材料二可推知氯化钾、氯化镁、氯化铝三种物质中有一种物质是不符合题意的,这种物质是________,其理由是________.
(2)有人认为材料一中的题干正确,只要把一个正确的选项补加进去就是一道好题,你认为选项改加“(Ⅰ)0∶0∶0”和“(Ⅱ)6∶3∶0”哪个好?________(填写编号)
(3)也有人认为只要把氯化钾、氯化镁、氯化铝中的其中一种物质改为材料二表格中另一种物质也符合题意.写出电解这种物质的化学方程式:________
(6分)25℃时,有0.01 mol•L-1的醋酸溶液,(1)醋酸的电离平衡常数表达式
达平衡时,溶液中氢离子浓度是 (25℃时,醋酸的电离平衡常数为1. 75×10 -5)
当向该溶液中加入一定量的盐酸时,电离常数 发生变化(填是否)
 CHR′与碱性KMnO4溶液共热后酸化,发生双键断裂生成羧酸:
CHR′与碱性KMnO4溶液共热后酸化,发生双键断裂生成羧酸: CHR′
CHR′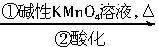 RCOOH+R′COOH
RCOOH+R′COOH C键化合物的结构。
C键化合物的结构。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com