
题目列表(包括答案和解析)

| 催化剂 |
| 加热 |
| 催化剂 |
| 加热 |

 萤光素(X)常用于钞票等防伪印刷,下列关于它的说法不正确的是( )
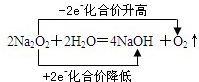
萤光素(X)常用于钞票等防伪印刷,下列关于它的说法不正确的是( )(12)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1) A中铁丝发生如下反应2Fe+3Br2=2FeBr3,FeBr3的作用是 ,请写出A中另外一个反应的化学方程式 。
(2)观察到 A中的气体颜色是由______色变成_______色。
A中的气体颜色是由______色变成_______色。
(3)实验结 束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________________________________。
束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________________________________。
(4)C中盛放CCl4的作用是____________________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应的方法是验证是否有HBr的生成,故而可向试管D中滴入石蕊溶液,若溶液变红,则能 证明。另一种验证的方法是向试管D中加入__________,现象是__________________________________________。
证明。另一种验证的方法是向试管D中加入__________,现象是__________________________________________。
(12)某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如图所示(部分反应物或生成物未列出),其中E为白色沉淀,I为红褐色沉淀。

(1)写出下列物质的化学式:F____________________,G_______________
(2)分离粉末状混合物最简单的方法是__________________________________
(3)D→E转化中,加入足量的X,试剂X可能是________
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:_____________________________________________________________________
H→I:____________________________________________________________________
(5)过量的B加入稀硝酸中的化学反应方程式为:____________________________________
(6)若对G溶液中的阳离子进行检验:用所给试剂(KSCN溶液、氯水)设计检验G溶液中阳离子的方法。
。
(12分)某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
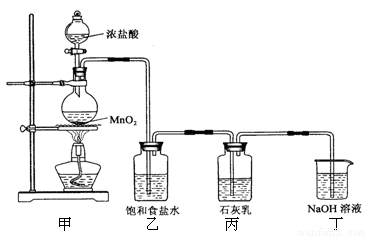
请回答下列问题:
(1)①甲装置用于制备氯气,其反应的化学方程式是 ;乙装置的作用是______。
②该兴趣小组用100mL 12mol/L盐酸与 8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2______________g。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢。匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。①图中曲线I表示_____________离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为______________mol。

(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:______。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com