
题目列表(包括答案和解析)
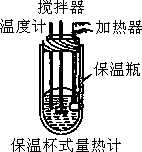
在量热计中(如图)将100mL 0.50mol/L的![]() 溶液与100mL 0.55mol/L
溶液与100mL 0.55mol/L![]() 溶液混合,温度从298.0K升高到300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J/K,溶液密度均为1g/mL,生成溶液的比热容
溶液混合,温度从298.0K升高到300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J/K,溶液密度均为1g/mL,生成溶液的比热容![]() J/(g·K).
J/(g·K).
(1)试求![]() 的中和热
的中和热![]() .
.
(2)![]() 的中和热的文献值为-56.1kJ/mol,你认为(1)中测得的实验值偏差可能的原因是__________________.
的中和热的文献值为-56.1kJ/mol,你认为(1)中测得的实验值偏差可能的原因是__________________.
(3)实验中![]() 过量的目的是________________.
过量的目的是________________.
(4)你认为![]() 的中和热与
的中和热与![]() 的中和热数值相比,________较大,其原因是________________________.
的中和热数值相比,________较大,其原因是________________________.
反应速度V和反应物浓度的关系是用实验方法测定的。化学反应H2+Cl2→2HCl的反应速度V可表示为V=K![]() 式中K为常数,m.n值可用下表中数据确定之。
式中K为常数,m.n值可用下表中数据确定之。
|
|
| V(mol/L?s) |
| 1.0 | 1.0 | 1.0K |
| 2.0 | 1.0 | 2.0K |
| 2.0 | 4.0 | 4.0K |
由此可推得,m.n值正确的是 ( )
A.m=1.n=1 B.m=![]() .n=
.n=![]() C.m=
C.m=![]() .n=1 D.m=1.n=
.n=1 D.m=1.n= ![]()
反应速率v和反应物浓度的关系是用实验方法测定的。化学反应H2+Cl2=2HCl的反应速率v可表示为v = k[c(H2)]m[c(Cl2)]n,式中k为常数,m、n值可用下表中数据确定之。
| c (H2)(mol/L) | c (Cl2) (mol/L) | v [mol/(L·s)] |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
由此可推得,m、n值正确的是 ( )
A. m=1、n=![]() B.m=
B.m=![]() 、n=
、n=![]() C.m=
C.m=![]() 、n=1 D. m=1、n=1
、n=1 D. m=1、n=1
| c(H2)mol/L | c(Cl2)mol/L | v/mol/L?s |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
| A、m=1 n=1 | ||||
B、m=
| ||||
C、m=
| ||||
D、m=1 n=
|
| A.水煤气只能用作燃料 |
| B.水煤气是一种二级能源.比煤直接燃烧污染小 |
| C.等质量的CO和H2完全燃烧时,前者放热多 |
| D.因△H1>0,煤气化后再燃烧比煤直接燃烧放出热量少 |
一、选择题(每小题只有一个选项符合题意,每小题2分,共40分)
题 号
1
2
3
4
5
6
7
8
9
10
答 案
D
A
D
C
B
B
C
C
A
A
题 号
11
12
13
14
15
16
17
18
19
20
答 案
C
A
A
D
C
D
A
C
D
D
二、实验题: (本大题包括2小题,共18分)
21、(1)铁屑溶解,溶液逐渐变为浅绿色,有大量无色气泡产生(2分)
杂质Cu与Fe形成原电池,化学反应速率加快(2分)
(2)2FeC12+2HC1+H2O2=2FeC13+2H2O(2分)
(3)在HCl气氛中加热浓缩,冷却结晶,过滤(2分)
FeC13+3H2O Fe(OH)3 + 3HCl;直接加热时,FeC13水解会产生Fe(OH)3
(2分)
Fe(OH)3 + 3HCl;直接加热时,FeC13水解会产生Fe(OH)3
(2分)
(4)B(2分)
22、(1)A(2分) (2)2H++ 2e-= H2↑ (2分)
(3)2Fe3++ Fe = 3Fe2+ (2分)
三、填空题:(本大题共4小题。共36分)
23、(1)⑤⑥(2分) ①④⑧(2分)
(2)2Fe3++3CaCO3+3H2O = 2Fe(OH)3+3Ca2++3CO2↑ (2分)
或;2Fe3++3H2O Fe(OH)3+3H+ CaCO3+2H+ =
Ca2++H2O+3CO2↑
Fe(OH)3+3H+ CaCO3+2H+ =
Ca2++H2O+3CO2↑
(3)HCO3-+A1O2-+H2O=Al(OH)3↓+CO32-(2分)
24、(1)B(2分) ;
(2)CH3COONH4溶液呈中性,滴入Mg(OH)2 悬浊液,若Mg(OH)2溶解,则说明乙同学解释正确,若Mg(OH)2不溶,则甲同学解释正确。(2分)
(3)乙(2分);Mg(OH)2 + 2NH4+ ㄔ Mg2+ + 2NH3?H2O(2分)
25、(1)A、D(2分)
(2)用湿润的红色石蕊试纸放在管口处,若试纸变蓝说明有氨气生成。(2分)
(3)该反应是可逆反应,10mol N2与30mol H2不能完成反应,所以放出的热量小于924kJ。(2分)
(4)N2+6H++6e-=2NH3(2分)
26、(1)0.05(2分), 25 (2分)
(2) H2SO4与(NH4)2SO4(2分), (NH4)2SO4与NH3?H2O(2分)(本小题若其它合理答案也给分)
(3)=7 (2分) (4)BC (2分)
四、计算题:(本大题共6分)27、AgI(2分)、AgCl(2分)、4.1×10-14mol/L(2分)
附加题:
28、(1)BiCl3+H2O=BiOCl↓+2HCl(2分)
(2)不合理 (2分) 因BiOCl中Cl呈-1价而非+1(2分)
(3)将BiCl3溶于含适量HCl的蒸馏水中(2分)
(4)BiOCl+H2O BiOCl+2H++2Cl-,[Cl-]增大时,抑制了BiCl3水解(2分)
BiOCl+2H++2Cl-,[Cl-]增大时,抑制了BiCl3水解(2分)
29、(1) 正反应 (2分) 7.0 (2分)
(2) 不相等(2分) 因为这两种情况是在两个不同温度下达到化学平衡的(2分),平衡状态不同,所以物质的量也不同(2分)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com