
题目列表(包括答案和解析)

回答下列问题:
(1)化合物E、M的沸点____________高(填化学式),原因是_______________________。
(2)甲、乙两种元素还可以形成一种含有4个原子核和18个电子的化合物,该化合物的结构式为_________________________________。
(3)E与D高温反应的化学方程式为________________________,K与M在水溶液中反应的离子方程式为____________________________________________。
(4)实验室在保存L溶液时,需加入少量D,理由是________________________,实验室检验L的水溶液中的阳离子的方法是________________________________________。
(5)已知一定条件下每1 mol F与单质B完全反应生成I放热98.0 kJ,若2 mol F与1 mol B在此条件下发生反应,达平衡时,放出热量为176.4 kJ,则F的转化率为____________,平衡时F的物质的量为____________,若保持温度和压强不变(反应混合物都为气体)按下列四种配比作为起始物质充入,达到平衡时各物质的物质的量与上述平衡状态相同的是_______________。
A.4 mol F 2 mol B
B.2 mol F 1 mol B 2 mol I
C.1 mol F 0.5 mol B 1 mol I
D.3 mol I 1 mol Ne
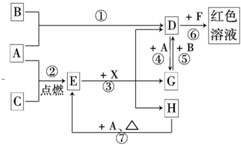 A、B、C为中学常见单质,其中一种为金属;通常情况下,A为固体,B为液体,C为气体.D、E、F、G、H、X、Y均为化合物,其中X是一种无氧强酸、E为黑色晶体,H在常温下为液体.它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去).
A、B、C为中学常见单质,其中一种为金属;通常情况下,A为固体,B为液体,C为气体.D、E、F、G、H、X、Y均为化合物,其中X是一种无氧强酸、E为黑色晶体,H在常温下为液体.它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去).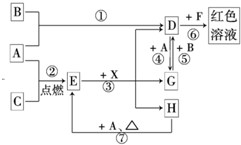
已知A为蓝色溶液,B、C、I、K为单质,其余均为化合物,其中B、L、I、K 常温下为气体,且只有I为有色气体。G为黑色固体,F的焰色反应透过蓝色钻玻璃片显紫色,各物质转化关系如图。
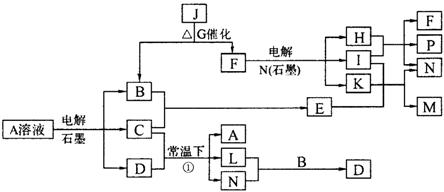
回答下列问题:
(1)F的电子式:____________;
(2)写出反应①的化学反应方程式: ;
(3)用惰性电极电解足量A溶液,一段时间后,若要使溶液恢复到电解前的状态,则可向溶液中加入适量___________或__________。
(4)已知B、H和C2H5OH能够组成燃料电池,写出该燃料电池的负极电极反应方程式: ;
第Ⅰ卷(选择题,共45分)
题号
1
2
3
4
5
6
7
8
答案
B
A
D
B
C
D
A
D
题号
9
10
11
12
13
14
15

答案
B
C
C
D
B
A
C

第Ⅱ卷(非选择题,共55分)
二.(本大题包括2小题,计14分)
16.(8分)(1)变大(1分) 变小 (1分)
(2)NH4Cl(2分)NH3?H2O(2分)c(NH4+)=c(Cl-)>c(H+)=c(OH-)(2分)
17.(6分)(1)2NH3 NH4
NH4 +
NH2
+
NH2 (2分)
(2分)
(2)AE(2分)
(3)Al3+(2分)
三.(本大题包括2小题,计18分)
18.(10分)(1)  (2分)
(2分)  (2分)
(2分)
(2)Mg (2分)O=C=O(2分) 2Mg+CO2
(2分)O=C=O(2分) 2Mg+CO2 2MgO+C (2分)
2MgO+C (2分)
19.(8分)(1)三角锥型(2分)
(2) Al-3e-=Al3+或Al-3e-+30H-=Al(0H)3(2分) 02+4e-+2H20=40H- (2分)
(3) Al(0H)3+0H-=AlO2-+2H20(2分)
四.(本大题包括2小题,计23分)
20.(10分)(1)O22-+H2O HO2-+OH-(2分)
HO2-+OH-(2分)
(2) H2O2 (2分)
(3)HO2-+H+= H2O2 2H2O2 2H2O+O2↑(各2分,合理答案参照给分)
2H2O+O2↑(各2分,合理答案参照给分)
(4)B(2分)
21.(13分)(1)Cu在Cl2中燃烧生成棕色烟(2分)
(2)Fe在冷浓硝酸中发生钝化(2分)3:1(2分)
(3)①试管内出现红棕色气体或铜片表面有气泡生成(2分)
②Fe和硝酸反应后的溶液中有HNO3,也一定有Fe3+,而Fe3+也能和Cu反应,使Cu片溶解(2分)
(4)取少许该溶液滴加几滴KSCN溶液,不出现血红色,再滴加适量新制氯水,出现血红色(3分,合理答案参照给分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com