
题目列表(包括答案和解析)
A.Fe3+、NO 、Cl-、Na+ 、Cl-、Na+ | B.Ca2+、HCO 、Cl-、K+ 、Cl-、K+ |
C.NH 、Fe2+、SO 、Fe2+、SO 、NO 、NO | D.Cl-、SO 、K+、Na+ 、K+、Na+ |
A.Al3+、NO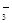 、OH-、Cl- 、OH-、Cl- | B.H+、Ba2+、Ag+、Cl- |
C.Fe2+、Fe3+、Na+、NO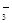 | D.Ca2+、H+、Cl-、CO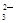 |
下列各组中的离子,能在溶液中大量共存的是( )
A.Al3+、NO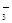 、OH-、Cl- 、OH-、Cl- | B.H+、Ba2+、Ag+、Cl- |
C.Fe2+、Fe3+、Na+、NO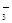 | D.Ca2+、H+、Cl-、CO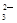 |
A.C6H5O-、Cl-、Na+、Fe3+ B.SCN-、Fe3+、K+、NO![]()
C.Fe3+、MnO![]() 、Cu2+、Cs+ D.Br-、F-、Ba2+、Ca2+
、Cu2+、Cs+ D.Br-、F-、Ba2+、Ca2+
在下列各溶液中,离子一定能大量共存的是( )
A.强碱性溶液中:K+、Al3+、Cl-、SO![]()
B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、SCN-、NO![]()
C.含有0.1 mol·L-1 Ca2+的溶液中:Na+、K+、CO![]() 、Cl-
、Cl-
D.室温下,pH=1的溶液中:Na+、Fe3+、NO![]() 、SO
、SO![]()
难点磁场
提示:根据电荷守恒,可知A错B对。根据由水电离产生的H+和OH-个数相等,可知C对。根据Na2S中,Na+个数是S2-的两倍,可知D对。
答案:BCD
歼灭难点训练
1.提示:常温下,c(H+)=1.0×10-7 mol?L-1,即每升水中已电离的水的物质的量是1.0×10-7 mol,而每升水的物质的量是 ,则:
,则:
n= mol∶10-7 mol=5.56×108
mol∶10-7 mol=5.56×108
答案:B
2.提示:本题有两种解法。
方法1(常规解法):NaOH(aq)中:
c水(OH-)=c水(H+)= mol?L-1=1.0×10-5 mol?L-1
mol?L-1=1.0×10-5 mol?L-1
CH3COONa(aq)中:
c′水(OH-)=c′总(OH-)=10-9 mol?L-1
则A∶B=10-4
方法2(巧解法):NaOH(aq)中,水的电离被抑制;CH3COONa(aq)中,水的电离被促进;故A<B。
答案:B
3.提示:c水(H+)=1.0×10-13 mol?L-1,则该溶液可能是强碱性溶液,也可能是强酸性溶液,总之,水的电离被抑制。因而“一定不可能大量存在”是指酸性和碱性条件下都不能大量存在。
答案:BC
评注:若去掉题干中的“不可”,则选D。若去掉题干中的“一定不”,则选AD。
4.提示:Na3PO4完全电离,水部分电离:
Na3PO4====3Na++PO
H2O H++OH-
H++OH-
PO 发生系列水解:
发生系列水解:
PO +H2O
+H2O HPO
HPO +OH-
+OH-
HPO +H2O
+H2O H2PO
H2PO +OH-
+OH-
H2PO +H2O
+H2O H3PO4+OH-
H3PO4+OH-
答案:8
(1)c(Na+)+c(H+)==c(OH-)+3c(PO )+2c(HPO
)+2c(HPO )+c(H2PO
)+c(H2PO )
)
(2)c(H+)+c(HPO )+2c(H2PO
)+2c(H2PO )+3c(H3PO4)==c(OH-)
)+3c(H3PO4)==c(OH-)
(3)c(Na+)==3c(PO )+3c(HPO
)+3c(HPO )+3c(H2PO
)+3c(H2PO )+3c(H3PO4)
)+3c(H3PO4)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com