
题目列表(包括答案和解析)

各举一例写出转化的化学方程式:
①___________________________________________________________________;
②___________________________________________________________________;
③___________________________________________________________________;
④___________________________________________________________________;
⑤___________________________________________________________________;
⑥___________________________________________________________________。
(10分) 有三种物质AC2、B2C2、AD4,第二周期元素A的最高正价和负价绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;元素D的负一价阴离子电子层结构与氩原子相同,则:
(1)A、B、C的元素名称分别为 、 、 。
(2)AD4分子其中含有的σ键类型为 (选填“s-sσ键”、“s-p σ键”或“p-pσ键”)。键角为 , AD4的等电子体有 。
(3)D的负一价阴离子的电子排布式为 ,B2C2的电子式为 ,属 (填“离子化合物”或“共价化合物”)。1mol B2C2与足量AC2反应转移的电子个数为 。
(10分)有三种物质AC2、B2C2、AD4,第二周期元素A的最高正价和负价绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;元素D的负一价阴离子电子层结构与氩原子相同,则:
(1)A、B、C的元素名称分别为 、 、 。
(2)AD4分子其中含有的σ键类型为 (选填“s-sσ键”、“s-p  σ键”或“p-pσ键”)。键角为 , AD4的等电子体有 。
σ键”或“p-pσ键”)。键角为 , AD4的等电子体有 。
(3)D的负一价阴离子的电子排布式为 ,B2C2的电子式为 ,属 (填“离子化合物”或“共价化合物”)。1mol B2C2与足量AC2反应转移的电子个数为 。
(20分)某化学课外活动小组以铝屑、稀H2SO4、NaOH溶液为主要原料欲制备Al(OH)3沉淀,设计了如下三种方案,见下表。阅读下表并回答下列问题:
| 途径 | 生成1 mol Al(OH)3消耗H+或OH-的物质的量/mol | |
| 消耗H+ | 消耗OH- | |
| 1.Al→Al3+→Al(OH)3 | | |
2.Al→AlO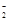 →Al(OH)3 →Al(OH)3 | | |
3.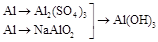 | | |
 (g)NaOH固体。他在托盘天平的右盘上放入(
(g)NaOH固体。他在托盘天平的右盘上放入( + y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使 。
+ y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使 。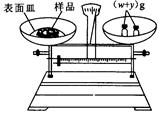
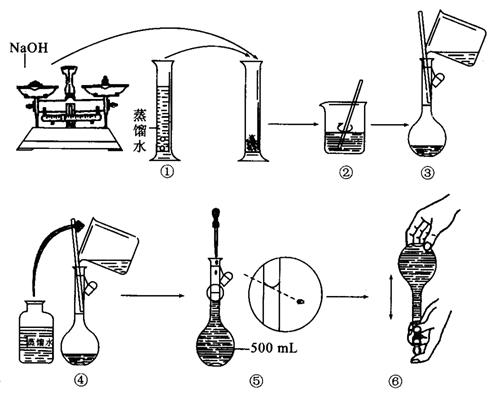
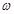 (g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。
(g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。
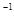 NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。
NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。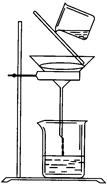
(20分)某化学课外活动小组以铝屑、稀H2SO4、NaOH溶液为主要原料欲制备Al(OH)3沉淀,设计了如下三种方案,见下表。阅读下表并回答下列问题:
|
途径 |
生成1 mol Al(OH)3消耗H+或OH-的物质的量/mol |
|
|
消耗H+ |
消耗OH- |
|
|
1.Al→Al3+→Al(OH)3 |
|
|
|
2.Al→AlO |
|
|
|
3. |
|
|
(1)填写上表中空格并从节约原料的角度来分析,你认为应选择方案_________最为合理。
(2)本实验要用到NaOH溶液。某学生用已知质量y(g)的表面皿,准确称取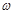 (g)NaOH固体。他在托盘天平的右盘上放入(
(g)NaOH固体。他在托盘天平的右盘上放入(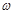 + y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使
。
+ y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使
。
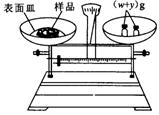
(3)若称取的 (g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。
(g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。
(4)阅读下列制备Al(OH)3实验步骤,填写空白:
①在烧杯A中加入50mL0.5mol·L NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。
NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。
②在盛有适量稀H2SO4的烧杯B中应放入___________(g)(用含m1的式子表示)质量的铝屑,充分搅拌使铝屑反应完全。
③在盛有适量浓NaOH溶液的烧杯C中放入____________(g)(用含m1的式子表示)质量的铝屑充分搅拌使铝屑反应完全。
④将烧杯B和烧杯C中的溶液混和观察到的现象是:_______________________________,反应的离子方程式是:___________________________
(5)过滤时某学生操作如图,请用文字说明图中错误的是:
_____________________ 。

(6)把沉淀转移到烧杯中,用蒸馏水洗涤三次再过滤,再洗涤、
干燥得Al(OH)3固体质量为m2(g)计算本实验Al(OH)3的产率是_________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com