
题目列表(包括答案和解析)
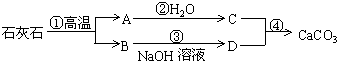
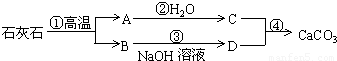
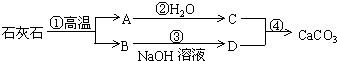

石灰石是我市最丰富的矿藏之一,用途极为广泛。除了可以用于生产生石灰和水泥外,工业上还常常用沉淀法生产碳酸钙。用这种方法得到的碳酸钙是一种极细的粉末,在工业又称为轻质碳酸钙,是一种重要的工业原料,具有很高的经济价值。我市某工厂利用下列工艺流程生产轻质碳酸钙:
![]()
请根据以上信息回答下列问题:
⑴ 工厂每天用16吨含碳酸钙65%的石灰石作为原料,如果碳酸钙在高温下全部分解,可得到多少吨生石灰?[假设石灰石中的杂质在高温下不发生化学反应,计算结果保留一位小数]
⑵ 氢氧化钠是上述生产轻质碳酸钙工艺流程中的副产品,工厂为了提高经济效益,通常回收氢氧化钠固体出售。现市场上氢氧化钠固体的价格为每吨3400元,如果该工厂每天生产10吨轻质碳酸钙,试计算工厂每天可从出售氢氧化钠固体中得到多少收入?
⑶ 根据初中已学的知识,如果还是用石灰石作为原料,请你写出另一种制取轻质碳酸钙的方案。对照题给的生产轻质碳酸钙工艺流程,议一议你设计的方案是否适宜工业上生产,有什么优缺点。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com