
题目列表(包括答案和解析)
[2012·临沂一模](10分)下列转化关系所涉及的物质都是中学化学常见物质。已知A、B为氧化物,C为固体单质,D为黄绿色气体。
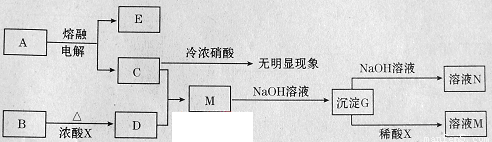
请回答:
(1)指出A中存在的化学键类型: 。
(2)写出M与过量氨水反应的离子方程式: 。
(3)向溶液N中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是
_____________ ________。
(4)电解熔融氧化物A,阳极的电极反应方程式为 。
(5)B与浓酸X反应的化学方程式为 。
(6)能不能直接蒸发溶液M得到M晶体? (填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作? 。
[2012·临沂一模](10分)下列转化关系所涉及的物质都是中学化学常见物质。已知A、B为氧化物,C为固体单质,D为黄绿色气体。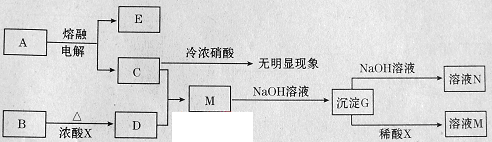
请回答:
(1)指出A中存在的化学键类型: 。
(2)写出M与过量氨水反应的离子方程式: 。
(3)向溶液N中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是
_____________ ________。
(4)电解熔融氧化物A,阳极的电极反应方程式为 。
(5)B与浓酸X反应的化学方程式为 。
(6)能不能直接蒸发溶液M得到M晶体? (填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作? 。
下列转化关系所涉及的物质都是中学化学常见物质。已知A、B为氧化物,C为固体单质,D为黄绿色气体。

请回答:
(1)指出A中存在的化学键类型: 。
(2)写出M与过量氨水反应的离子方程式: 。
(3)向溶液N中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是
_____________ ________。
(4)电解熔融氧化物A,阳极的电极反应方程式为 。
(5)B与浓酸X反应的化学方程式为 。
(6)能不能直接蒸发溶液M得到M晶体? (填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作? 。
下列转化关系所涉及的物质都是中学化学常见物质。已知A、B为氧化物,C为固体单质,D为黄绿色气体。
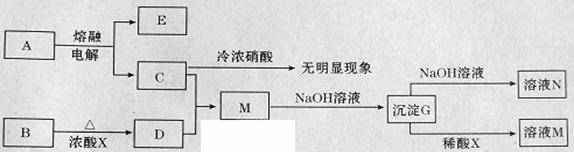
请回答:
(1)指出A中存在的化学键类型: 。
(2)写出M与过量氨水反应的离子方程式: 。
(3)向溶液N中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是
_____________ ________。
(4)电解熔融氧化物A,阳极的电极反应方程式为 。
(5)B与浓酸X反应的化学方程式为 。
(6)能不能直接蒸发溶液M得到M晶体? (填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作? 。
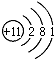
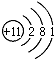
| ||
| ||
一、单项选择题(本题包括12小题,每小题4分,共48分。每小题只有一个选项符合题意)
题号
1
2
3
4
5
6
7
8
9
10
答案
D
B
D
A
B
A
C
B
D
C

 22.(14分)
(1) O、H、S、Cl 硫酸(4分)
22.(14分)
(1) O、H、S、Cl 硫酸(4分)
(2) (3分)
(3) SO2 + 2H2O + Cl2 = 4H++ SO42-+ 2Cl-(3分)
SO2和Cl2按相等物质的量通入品红溶液(2分)
(4) Fe + S
 FeS,2Fe + 3Cl2
FeS,2Fe + 3Cl2
 2FeCl3(或Cl2 +
H2S = S↓+ 2HCl
2FeCl3(或Cl2 +
H2S = S↓+ 2HCl
或Cl2 + Na2S S↓+ 2NaCl)(2分)
四、实验题(本大题共2小题,共21分)
23.(5分)
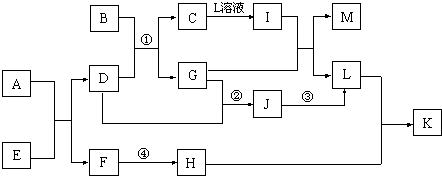
(1)同周期
(2)同主族
Ⅰ
A、F、H
E、D
Ⅱ
d、c、b
g、f
24.(16分) (1) 分液漏斗上口的塞子未打开(或漏斗未与大气相通或漏斗塞子的凹槽未与颈部的通气孔对准。(2分)
(2) ④ (2分)
(3) 溶液由红色褪为无色,SO2 + OH- = HSO3-或SO2 + 2OH-= SO32-+ H2O。 (4分)
(4) 产生白色沉淀,SO2被HNO3氧化产生SO42-,与Ba2+产生白色沉淀。(4分)
(5) ① 关闭K2,在烧杯中用水封住玻璃导管口,用手捂住集气瓶b,烧杯中导管口有气泡产生,松手后,导管内有一段液柱保持不降则气密性好。(2分)
② 打开K1,关闭K2,点燃酒精灯。(2分)
五、计算题(本大题共1个小题,共11分)
25.(1) S H2S Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S↓+ H2O
Na2S + H2SO4 = Na2SO4 + H2S↑ 2H2S+SO2=3S↓+2H2O(各1分)
(2) Na2S2O3 :0.025 mol Na2S:0.075 mol(各3分)
本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com