
题目列表(包括答案和解析)
以水氯镁石(主要成分为![]() )为原料生产碱式碳酸镁的主要流程如下:
)为原料生产碱式碳酸镁的主要流程如下:

(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的![]() ,若溶液中
,若溶液中![]() ,则溶液中
,则溶液中![]() = 。
= 。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。
(3)高温煅烧碱式碳酸镁得到![]() 。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下![]() 0.896L,通过计算确定碱式碳酸镁的化学式。
0.896L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有![]() ,则产品中镁的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
,则产品中镁的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
 以水氯镁石(主要成分为
以水氯镁石(主要成分为![]() )为原料生产碱式碳酸镁的主要流程如下:
)为原料生产碱式碳酸镁的主要流程如下:
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的 ,若溶液中
,若溶液中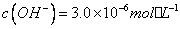 ,则溶液中
,则溶液中 = 。
= 。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。
(3)高温煅烧碱式碳酸镁得到![]() 。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下![]() 0.896L,通过计算确定碱式碳酸镁的化学式。
0.896L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有![]() ,则产品中镁的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
,则产品中镁的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
 以水氯镁石(主要成分为
以水氯镁石(主要成分为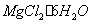 )为原料生产碱式碳酸镁的主要流程如下:
)为原料生产碱式碳酸镁的主要流程如下:
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的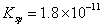 ,若溶液中
,若溶液中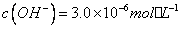 ,则溶液中
,则溶液中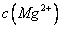 =
。
=
。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。
(3)高温煅烧碱式碳酸镁得到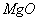 。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下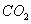 0.896L,通过计算确定碱式碳酸镁的化学式。
0.896L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有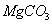 ,则产品中镁的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
,则产品中镁的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
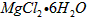 )为原料生产碱式碳酸镁的主要流程如下
)为原料生产碱式碳酸镁的主要流程如下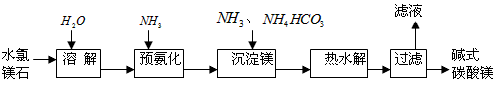
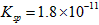 ,若溶液中
,若溶液中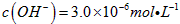 ,则溶液中
,则溶液中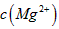 =_______________。
=_______________。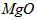 。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下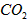 0.896L,通过计算确定碱式碳酸镁的化学式。__________________________
0.896L,通过计算确定碱式碳酸镁的化学式。__________________________ 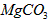 ,则产品中镁的质量分数_____________(填 “升高”、“降低”或“不变”)。
,则产品中镁的质量分数_____________(填 “升高”、“降低”或“不变”)。 以水氯镁石(主要成分为![]() )为原料生产碱式碳酸镁的主要流程如下:
)为原料生产碱式碳酸镁的主要流程如下:
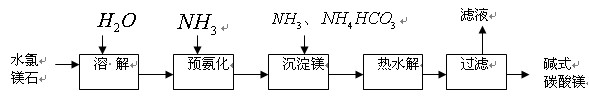
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的![]() ,若溶液中
,若溶液中![]() ,则溶液中
,则溶液中![]() = 。
= 。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。
(3)高温煅烧碱式碳酸镁得到![]() 。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下![]() 0.896L,通过计算确定碱式碳酸镁的化学式。
0.896L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有![]() ,则产品中镁的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
,则产品中镁的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com