
题目列表(包括答案和解析)

物质A有如下图所示转化关系,其中乙为金属单质,常温下,它在G的浓溶液中发生钝化,F的溶液中只含有一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明).请讨论以下两种情况(注:两种情况下各字母代表的物质可能不同)
回答下列问题:
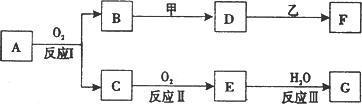
(1)第一种情况:用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质;D和F的溶液均呈碱性.则:
①反应Ⅲ的化学方程式为________.
②D与乙反应的离子方程式为________
(2)第二种情况:甲由两种单质直接化合得到;B为红棕色固体;C为无色气体,是形成酸雨的大气污染物之一;D的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成.则:
①工业上,反应I的化学方程式为________
生产设备名称为:________
②D和乙反应的离子方程式为________
③请简述检验D溶液中阳离子的方法________.
④若A的相对分子质量为120,反应Ⅰ、Ⅱ、Ⅲ均为完全转化.现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρ g/cm3,溶质质量分数为a%的G溶液n mL.则该样品中A的质量分数=________(列出计算式即可).
(10分)物质A~Z有下图所示的转化关系(部分反应物与产物已略去)。其中,常温下B、C为气体单质,Y为固体单质,Y是电子工业中常用的半导体材料。F是具有磁性的黑色晶体。E的水溶液与M混合后得到N,N经过干燥脱水可得到一种常用于实验室和袋装食品、瓶装食品等的干燥剂,K的焰色反应为紫色,A的焰色反应为黄色。
请回答:
(1)利用①反应进行化工生产的工业名称为 ,K的化学式 ;D的电子式________________;
(2)反应①的离子方程式 ;
(3)向H的水溶液中加入足量氨水并将溶液露置在空气中,观察到的现象是 ;向相同体积相同浓度的两份G溶液中分别滴加相同PH的氨水和D溶液,当沉淀最大量时所加入的氨水和D溶液的体积分别为V1、V2,则V1、V2的大小关系V1 V2。
(4)写出反应⑥的化学方程式 。
(5)N为比碳酸还弱的酸,设计实验证明,简述实验过程和现象 。

物质A~Z有下图所示的转化关系(部分反应物与产物已略去)。其中,常温下B、C为气体单质,Y为固体单质,Y是电子工业中常用的半导体材料。F是具有磁性的黑色晶体。E的水溶液与M混合后得到N,N经过干燥脱水可得到一种常用于实验室和袋装食品、瓶装食品等的干燥剂,K的焰色反应为紫色,A的焰色反应为黄色。

请回答:
(1)利用①反应进行化工生产的工业名称为 ,K的化学式 ;D的电子式________________;
(2)反应①的离子方程式 ;
(3)向H的水溶液中加入足量氨水并将溶液露置在空气中,观察到的现象是 ;向相同体积相同浓度的两份G溶液中分别滴加相同PH的氨水和D溶液,当沉淀最大量时所加入的氨水和D溶液的体积分别为V1、V2,则V1、V2的大小关系V1 V2。
(4)写出反应⑥的化学方程式 。
(5)N为比碳酸还弱的酸,设计实验证明,简述实验过程和现象 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com