
题目列表(包括答案和解析)
I.目前,我国采用“接触法”制硫酸,设备如图所示:

(1)图中设备A的名称是_____________,该设备中主要反应的化学方程式为 ??????????? 。
(2)有关接触法制硫酸的下列说法中,不正确的是_____(填字母序号)。
A.二氧化硫的接触氧化在接触室中发生
B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫
C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失2%
D.B装置中反应的条件之一为较高温度是为了提高SO2的转化率
E.硫酸工业中在接触室安装热交换器是为了利用SO3转化为 H2SO4时放出的热量
II.纯碱是一种重要的化工原料。制碱工业主要有“氨碱法”(索尔维法)和“联合制碱法”(侯氏制碱法)两种工艺。请按要求回答问题:
(3)CO2是制碱工业的重要原料,“联合制碱法”中CO2的来源于 ,“氨碱法”中CO2来源于 。
(4)氨碱法的原子利用率(原子利用率=期望产物的总质量与生成物的总质量之比) ??????? 。
(5)写出“联合制碱法”有关反应的化学方程式:?????????????????????????????? 。
I.目前,我国采用“接触法”制硫酸,设备如图所示:
(1)图中设备A的名称是_____________,该设备中主要反应的化学方程式为 。
(2)有关接触法制硫酸的下列说法中,不正确的是_____(填字母序号)。
| A.二氧化硫的接触氧化在接触室中发生 |
| B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫 |
| C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失2% |
| D.B装置中反应的条件之一为较高温度是为了提高SO2的转化率 |

| A.二氧化硫的接触氧化在接触室中发生 |
| B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫 |
| C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失2% |
| D.B装置中反应的条件之一为较高温度是为了提高SO2的转化率 |

 +
+
| 浓硫酸 |
| △ |
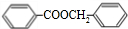 +H2O
+H2O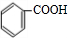 +
+
| 浓硫酸 |
| △ |
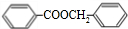 +H2O
+H2O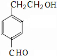

| 溶解性 | 沸点 | |
| A | 微溶于水 | 179.0℃ |
| E | 不溶于水 | 110.8℃ |
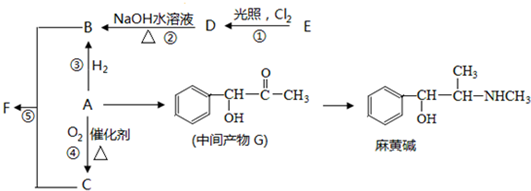
下图是中学化学常见物质的转化关系(某些反应条件及部分产物已略去),A、G为日常生活中的常见金属。B、C、E、I、J为气体,其中C为黄绿色气体,M为红褐色胶体。
 |
(1)已知A为第26号元素,请写出A元素在周期表中的位置__________
(2)D与G反应的化学方程式_________________________
(3)反应②离子方程式__________________________
(4)F→M的操作方法_______________
(5)现将一试管J气体倒立于水槽中一段时间后,水面上升但不充满;若使水充满整个试管,应向试管中通入一定量__________(填气体的化学式),此时试管中溶液的浓度为________mol/L(气体体积按标准状况计算)(保留两位有效数字)。
(6)①X、Y均为短周期元素,X最外层电子数比C气体所含元素最外层电子少1个且不同周期,Y与X同主族,下列关于X、Y、C三元素说法正确的是__________
A 原子半径 X〈 Y〈 C B 离子半径 X〈 C〈 Y
C 非金属性 X〈 Y〈 C D 最高价氧化物对应水化物酸性 C 〉X 〉Y
E 氢化物沸点 X〈 Y〈 C
② 请写出X的氢化物中原子个数比为1:1的化合物的电子式_________
(7)D与G反应生成A的同时,还有另一种产物,工业上用铝土矿(主要成分为Al2O3、、SiO2、Fe2O3)提取其的工艺流程如下:
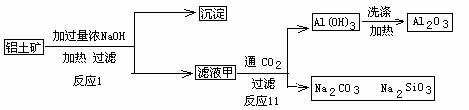 |
结合反应II,判断下列微粒结合质子(H+)的能力由强到弱的顺序是_________(填字母序号)
A. AlO2— B. OH— C. SiO32—
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com