
题目列表(包括答案和解析)
 I.已知:
I.已知: ,如果要合成
,如果要合成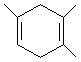 ,所用的原料可以是
,所用的原料可以是

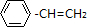
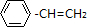



 CH2=CHCl
CH2=CHCl CH2=CHCl
CH2=CHCl

| A、C60与棒碳中所有的化学键都是非极性共价键 | B、棒碳不能使溴水褪色 | C、C60在一定条件下可能与CuO发生置换反应 | D、棒碳与乙炔互为同系物 |
(12分)已知在常用催化剂(如铂、钯)的催化下,氢气和炔烃加成生成烷烃,难于得到烯烃,但使用活性较低的林德拉催化剂[Pd/(PbO、CaCO3),其中钯附着于碳酸钙及少量氧化铅上],可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化。现有一课外活动兴趣小组利用上述原理设计了一套由如下图所示仪器组装而成的实验装置(铁架台未画出),拟由乙炔制得乙烯,并测定乙炔氢化的转化率。若用含0.020molCaC2的电石和1.60g含杂质18.7%的锌粒(杂质不与酸反应)分别与足量的X和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到的水VmL。试回答有关问题:
(1)装置的连接顺序是a、 、 、 、 、 、 、h(填各接口的字母)。
(2)写出A中所发生反应的化学方程式(有机物写结构简式): 。
(3)D的作用是___________________。
(4)为减慢A中的反应速率,X应选用____________________________。
(5)F中留下的气体除含少许空气外,还有__ __。G所选用的量筒的容积较合理的是_____。
A.500mL B.1000mL C.2000mL
(6)乙炔氢化的转化率为(用V来表示)_______________。
根据以上叙述完成(1)、(2)两小题。
(1)对于C60与棒碳,下列说法正确的是( )
A.C60在一定条件下可能与CuO发生置换反应 B.棒碳不能使溴水褪色
C.C60与棒碳中所有的化学键都是非极性共价键 D.棒碳与乙炔互为同系物
(2)晶胞是晶体结构中可重复出现的最小的结构单元,C60晶胞结构如下图所示,下列说法正确的是( )

A.C60摩尔质量是720
B.C60与棒碳互为同素异形体
C.在C60晶胞中有14个C60分子
D.每个C60分子周围与它距离最近等距离的C60分子有12个
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com