
题目列表(包括答案和解析)

| ||
| △ |
| ||
| △ |
| ||
| ||
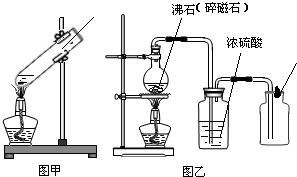
| 制取的气体 | 甲中盛放的试剂 | 乙中盛放的试剂 | 评价(回答是否可行,若不可行说明理由) |
| H2 | 锌粒和稀硫酸 | 浓H2SO4 | 不可行,因为氢气的密度比空气小,应用向下排空气法收集 不可行,因为氢气的密度比空气小,应用向下排空气法收集 |
| CO2 | 大理石和稀盐酸 | 浓NaOH溶液 | 不可行,因为二氧化碳与氢氧化钠溶液可反应,收集不到气体 不可行,因为二氧化碳与氢氧化钠溶液可反应,收集不到气体 |
| 步骤和方法 | 实验现象 | 分析与结论 |
| A:用燃着的火柴点燃干燥木条,一会儿木条燃烧,在火焰上方罩一干燥冷烧杯; 继续把火焰靠近烧杯底部. |
一会儿烧杯内壁有水雾产生; 一会儿烧杯底部出现一层黑色物质 |
木条中一定含有 氢 氢 元素;木条中一定含碳元素. |
| B:用燃着的火柴点燃干燥片状薄木片,木片很快燃烧,在火焰上方罩一干燥的冷烧杯; 继续把火焰靠近烧杯底部. |
一会儿烧杯内壁有水雾产生; 烧杯壁发热. |
木条中一定含有氧元素; 燃烧是放热反应. |
| 步骤和方法 | 实验现象 | 分析与结论 |
| 木条中一定含碳元素. 若发生反应,其化学方程式为 Ca(OH)2+CO2=CaCO3↓+H2O Ca(OH)2+CO2=CaCO3↓+H2O |
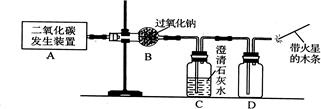 14、过氧化钠(化学式为Na2O2)可用在呼吸面具中作为氧气来源.Na2O2能跟CO2反应生成O2和另一种固体化合物 ( 用X表示 );也能跟H2O反应生成O2,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.以下是某兴趣小组进行的探究活动.
14、过氧化钠(化学式为Na2O2)可用在呼吸面具中作为氧气来源.Na2O2能跟CO2反应生成O2和另一种固体化合物 ( 用X表示 );也能跟H2O反应生成O2,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.以下是某兴趣小组进行的探究活动.| 实验操作 | 现 象 | 有关反应的化学方程式 |
| 方案一:取少量固体样品于试 管中,向其中 滴加稀盐酸,将气体通入澄清石灰水 . |
有气泡产生 ,澄清石灰水变浑浊 |
Na2CO3+2HCl=2NaCl+H2O+CO2↑ C02+Ca(OH)2=CaC03↓+H2O |
| 方案二:取少量固体,加水配 成溶液,滴加适量 氯化钙或氯化钡等 溶液 |
有白色沉淀产生 | Na2C03+CaCl2=CaC03↓+2NaCl 或Na2C03+BaCl2=BaC03↓+2NaCl等 |
 .
. .
.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com