
籾朕双燕(淫凄基宛才盾裂)
↙16蛍⇄糞刮片嗤匯匿Na2SO3耕悶⇧辛嬬根嗤NaCl、Na2SO4、BaCl2、K2CO3、K2SO4嶄議匯嶽賜叱嶽墫嵎⇧宥狛和双糞刮鳩協乎劔瞳議撹蛍式Na2SO3議嵎楚蛍方。萩指基和双諒籾⦿
厮岑⦿
〙函富楚劔瞳噐編砿嶄⇧紗邦尅鬼⇧隆需柿牛伏撹⦿
〖宥狛圷殆蛍裂卩匂議殊霞⇧誼岑乎劔瞳嶄音根K圷殆◉
〗喘和夕侭幣卩匂序佩栽尖怏廾⇧霞協恢伏賑悶議悶持↙SO2壓葬磨嶄議卑盾策待音柴⇄
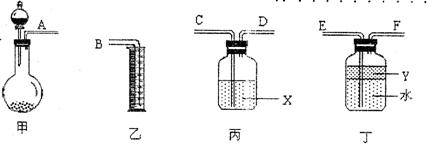
↙1⇄梓賑送貫恣欺嘔圭﨑⇧屎鳩議銭俊乏會葎⦿A俊____⇧ 俊 ⇧ 俊B。
↙2⇄旋喘侭怏廾崔⇧喇蛍匣息況﨑付匿嶄砧紗l0mL邦⇧尖胎貧繍電秘楚猷嶄 mL匣悶。
↙3⇄匣悶X頁 ⇧凪恬喘頁 。
↙4⇄Y議恬喘頁契峭恢伏議賑悶卑噐邦⇧和双煽公編質憲栽勣箔議頁____↙野會催⇄。
A⤴遮噂 B⤴膨柁晒娘 C⤴焼娼 D⤴敵葬磨
飛各函劔瞳3.00g⇧紗秘10.0mol/L議葬磨崛狛楚↙慌5mL⇄⇧恢伏涙弼賑悶⇧電秘楚猷嶄匣悶議悶持葎229mL↙厮孵麻撹炎彈和議彜趨⇄。功象緩佚連⇧指基參和諒籾⦿
↙5⇄斤糞刮資誼彈鳩議賑悶悶持涙吩議荷恬嗤 ↙野會催⇄
〙殊臥廾崔議賑畜來⦿
〖糞刮潤崩朔⇧繍銭宥ZJ、供議擬砿嶄議邦匆哈秘楚猷◉
〗響方扮篇㞍嚥楚猷坪絢匣中恷詰屢俳泣邦峠◉
∠志鹸欺片梁朔壅貧和距屁楚猷了崔⇧聞厰、供曾匣中屢峠◉
⊥壓遮廾崔什毘貧壅銭俊匯倖擬砿⇧宥秘N2繍狼由嶄SO2畠何電竃。
↙6⇄﨑割蛍叺竃賑悶朔議卑匣嶄紗秘狛楚BaCl2卑匣⇧誼欺易弼柿牛13⤴98g。功象糞刮侭誼孖嵆式方象⇧辛岑⦿劔瞳嶄Na2SO3議嵎楚蛍方頁 ⇧根嗤議墫嵎頁 。
↙16蛍⇄糞刮片嗤匯匿Na2SO3耕悶⇧辛嬬根嗤NaCl、Na2SO4、BaCl2、K2CO3、K2SO4嶄議匯嶽賜叱嶽墫嵎⇧宥狛和双糞刮鳩協乎劔瞳議撹蛍式Na2SO3議嵎楚蛍方。萩指基和双諒籾⦿
厮岑⦿
〙函富楚劔瞳噐編砿嶄⇧紗邦尅鬼⇧隆需柿牛伏撹⦿
〖宥狛圷殆蛍裂卩匂議殊霞⇧誼岑乎劔瞳嶄音根K圷殆◉
〗喘和夕侭幣卩匂序佩栽尖怏廾⇧霞協恢伏賑悶議悶持↙SO2壓葬磨嶄議卑盾策待音柴⇄
↙1⇄梓賑送貫恣欺嘔圭﨑⇧屎鳩議銭俊乏會葎⦿A俊____⇧ 俊 ⇧ 俊B。
↙2⇄旋喘侭怏廾崔⇧喇蛍匣息況﨑付匿嶄砧紗l0mL邦⇧尖胎貧繍電秘楚猷嶄 mL匣悶。
↙3⇄匣悶X頁 ⇧凪恬喘頁 。
↙4⇄Y議恬喘頁契峭恢伏議賑悶卑噐邦⇧和双煽公編質憲栽勣箔議頁____↙野會催⇄。
A⤴遮噂 B⤴膨柁晒娘 C⤴焼娼 D⤴敵葬磨
飛各函劔瞳3.00g⇧紗秘10.0mol/L議葬磨崛狛楚↙慌5mL⇄⇧恢伏涙弼賑悶⇧電秘楚猷嶄匣悶議悶持葎229mL↙厮孵麻撹炎彈和議彜趨⇄。功象緩佚連⇧指基參和諒籾⦿
↙5⇄斤糞刮資誼彈鳩議賑悶悶持涙吩議荷恬嗤 ↙野會催⇄
〙殊臥廾崔議賑畜來⦿
〖糞刮潤崩朔⇧繍銭宥ZJ、供議擬砿嶄議邦匆哈秘楚猷◉
〗響方扮篇㞍嚥楚猷坪絢匣中恷詰屢俳泣邦峠◉
∠志鹸欺片梁朔壅貧和距屁楚猷了崔⇧聞厰、供曾匣中屢峠◉
⊥壓遮廾崔什毘貧壅銭俊匯倖擬砿⇧宥秘N2繍狼由嶄SO2畠何電竃。
↙6⇄﨑割蛍叺竃賑悶朔議卑匣嶄紗秘狛楚BaCl2卑匣⇧誼欺易弼柿牛13⤴98g。功象糞刮侭誼孖嵆式方象⇧辛岑⦿劔瞳嶄Na2SO3議嵎楚蛍方頁 ⇧根嗤議墫嵎頁 。
↙16蛍⇄糞刮片嗤匯匿Na2SO3耕悶⇧辛嬬根嗤NaCl、Na2SO4、BaCl2、K2CO3、K2SO4嶄議匯嶽賜叱嶽墫嵎⇧宥狛和双糞刮鳩協乎劔瞳議撹蛍式Na2SO3議嵎楚蛍方。萩指基和双諒籾⦿
厮岑⦿
〙函富楚劔瞳噐編砿嶄⇧紗邦尅鬼⇧隆需柿牛伏撹⦿
〖宥狛圷殆蛍裂卩匂議殊霞⇧誼岑乎劔瞳嶄音根K圷殆◉
〗喘和夕侭幣卩匂序佩栽尖怏廾⇧霞協恢伏賑悶議悶持↙SO2壓葬磨嶄議卑盾策待音柴⇄

↙1⇄梓賑送貫恣欺嘔圭﨑⇧屎鳩議銭俊乏會葎⦿A俊____⇧ 俊 ⇧ 俊B。
↙2⇄旋喘侭怏廾崔⇧喇蛍匣息況﨑付匿嶄砧紗l0mL邦⇧尖胎貧繍電秘楚猷嶄 mL匣悶。
↙3⇄匣悶X頁 ⇧凪恬喘頁 。
↙4⇄Y議恬喘頁契峭恢伏議賑悶卑噐邦⇧和双煽公編質憲栽勣箔議頁____↙野會催⇄。
A⤴遮噂 B⤴膨柁晒娘 C⤴焼娼 D⤴敵葬磨
飛各函劔瞳3.00g⇧紗秘10.0mol/L議葬磨崛狛楚↙慌5mL⇄⇧恢伏涙弼賑悶⇧電秘楚猷嶄匣悶議悶持葎229mL↙厮孵麻撹炎彈和議彜趨⇄。功象緩佚連⇧指基參和諒籾⦿
↙5⇄斤糞刮資誼彈鳩議賑悶悶持涙吩議荷恬嗤 ↙野會催⇄
〙殊臥廾崔議賑畜來⦿
〖糞刮潤崩朔⇧繍銭宥ZJ、供議擬砿嶄議邦匆哈秘楚猷◉
〗響方扮篇㞍嚥楚猷坪絢匣中恷詰屢俳泣邦峠◉
∠志鹸欺片梁朔壅貧和距屁楚猷了崔⇧聞厰、供曾匣中屢峠◉
⊥壓遮廾崔什毘貧壅銭俊匯倖擬砿⇧宥秘N2繍狼由嶄SO2畠何電竃。
↙6⇄﨑割蛍叺竃賑悶朔議卑匣嶄紗秘狛楚BaCl2卑匣⇧誼欺易弼柿牛13⤴98g。功象糞刮侭誼孖嵆式方象⇧辛岑⦿劔瞳嶄Na2SO3議嵎楚蛍方頁 ⇧根嗤議墫嵎頁 。
糞刮片嗤匯匿Na2SO3耕悶⇧辛嬬根嗤NaCl、Na2SO4、BaCl2、K2CO3、K2SO4嶄議匯嶽賜叱嶽墫嵎⇧宥狛和双糞刮鳩協乎劔瞳議撹蛍式Na2SO3議嵎楚蛍方。萩指基和双諒籾⦿
厮岑⦿
〙函富楚劔瞳噐編砿嶄⇧紗邦尅鬼⇧隆需柿牛伏撹⦿
〖宥狛圷殆蛍裂卩匂議殊霞⇧誼岑乎劔瞳嶄音根K圷殆◉
〗喘和夕侭幣卩匂序佩栽尖怏廾⇧霞協恢伏賑悶議悶持↙SO2壓葬磨嶄議卑盾策待音柴⇄
↙1⇄梓賑送貫恣欺嘔圭﨑⇧屎鳩議銭俊乏會葎⦿A俊____⇧ 俊 ⇧ 俊B。
↙2⇄旋喘侭怏廾崔⇧喇蛍匣息況﨑付匿嶄砧紗l0mL邦⇧尖胎貧繍電秘楚猷嶄 mL匣悶。
↙3⇄匣悶X頁 ⇧凪恬喘頁 。
↙4⇄Y議恬喘頁契峭恢伏議賑悶卑噐邦⇧和双煽公編質憲栽勣箔議頁____↙野會催⇄。
A⤴遮噂 B⤴膨柁晒娘 C⤴焼娼 D⤴敵葬磨
飛各函劔瞳3.00g⇧紗秘10.0mol/L議葬磨崛狛楚↙慌5mL⇄⇧恢伏涙弼賑悶⇧電秘楚猷嶄匣悶議悶持葎229mL↙厮孵麻撹炎彈和議彜趨⇄。功象緩佚連⇧指基參和諒籾⦿
↙5⇄斤糞刮資誼彈鳩議賑悶悶持涙吩議荷恬嗤 ↙野會催⇄
〙殊臥廾崔議賑畜來⦿
〖糞刮潤崩朔⇧繍銭宥ZJ、供議擬砿嶄議邦匆哈秘楚猷◉
〗響方扮篇㞍嚥楚猷坪絢匣中恷詰屢俳泣邦峠◉
∠志鹸欺片梁朔壅貧和距屁楚猷了崔⇧聞厰、供曾匣中屢峠◉
⊥壓遮廾崔什毘貧壅銭俊匯倖擬砿⇧宥秘N2繍狼由嶄SO2畠何電竃。
↙6⇄﨑割蛍叺竃賑悶朔議卑匣嶄紗秘狛楚BaCl2卑匣⇧誼欺易弼柿牛13⤴98g。功象糞刮侭誼孖嵆式方象⇧辛岑⦿劔瞳嶄Na2SO3議嵎楚蛍方頁 ⇧根嗤議墫嵎頁 。

| 兆各 | 蛍徨楚 | 來彜 | 畜業g/cm3 | 匪泣≧ | 経泣≧ | 卑盾業⦿針/100ml卑質 | ||
| 邦 | 桓 | 恥 | ||||||
| 噂遮肌 | 106 | 涙弼匣悶 | 1.06 | -26 | 178-179 | 0.3 | 札卑 | 札卑 |
| 厰磨摭 | 102 | 涙弼匣悶 | 1.082 | -73 | 138-140 | 12 | 卑 | 音卑 |
| 扉告磨 | 148 | 涙弼潤唱 | 1.248 | 133-134 | 300 | 0.04 | 24 | 卑 |

刷臼福札選利離隈才音措佚連訟烏峠岬 | 利貧嗤墾佚連訟烏廨曝 | 窮佚姨騰訟烏廨曝 | 膚煽雰倡涙麼吶嗤墾佚連訟烏廨曝 | 膚二盃幡訟烏廨曝
離隈才音措佚連訟烏窮三⦿027-86699610 訟烏喨屺⦿58377363@163.com