
题目列表(包括答案和解析)

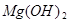 +2HCl=
+2HCl= +H2O)
+H2O)(3分)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如下图所示。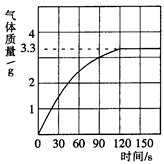
(友情提示: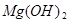 +2HCl=
+2HCl= +H2O)
+H2O)
(1)从图中可以看出,12.5g水垢与盐酸反应后生成的二氧化碳最多是 g。
(2)水垢中碳酸钙的质量分数是多少?
(3)假设水垢中除碳酸钙和氢氧化镁外,不含有其它杂质,溶解12.5 g水垢,至少需要质量分数为10%的盐酸的质量是 (最后结果保留一位小数)。
(3分)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如下图所示。
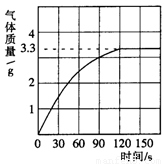
(友情提示: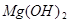 +2HCl=
+2HCl=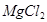 +H2O)
+H2O)
(1)从图中可以看出,12.5g水垢与盐酸反应后生成的二氧化碳最多是 g。
(2)水垢中碳酸钙的质量分数是多少?
(3)假设水垢中除碳酸钙和氢氧化镁外,不含有其它杂质,溶解12.5 g水垢,至少需要质量分数为10%的盐酸的质量是 (最后结果保留一位小数)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com