
籾朕双燕(淫凄基宛才盾裂)
(12蛍)(2009,表叫尖忝)ZnMnO2孤窮学哘喘鴻刑⇧凪窮盾嵎卑匣頁ZnCl2NH4Cl詞栽卑匣。
(1)乎窮学議減自可創頁________。窮学垢恬扮⇧窮徨送﨑________(野^屎自 ̄賜^減自 ̄)。
(2)飛ZnCl2NH4Cl詞栽卑匣嶄根嗤墫嵎Cu2⇦⇧氏紗堀蝶窮自議遣粉⇧凪麼勣圻咀頁___ _____________________________________________________________________。
圀茅肇Cu2⇦⇧恷挫僉喘和双編質嶄議________(野旗催)。
a⤴NaOH b⤴Zn
c⤴Fe d⤴NH3,H2O
(3)MnO2議伏恢圭隈岻匯頁參墳朝葎窮自⇧窮盾磨晒議MnSO4卑匣。咐自議窮自郡哘塀頁__________________。飛窮盾窮揃嶄宥狛2 mol窮徨⇧MnO2議尖胎恢楚葎________g。
(12蛍)(2009,表叫尖忝)ZnMnO2孤窮学哘喘鴻刑⇧凪窮盾嵎卑匣頁ZnCl2NH4Cl詞栽卑匣。
(1)乎窮学議減自可創頁________。窮学垢恬扮⇧窮徨送﨑________(野^屎自 ̄賜^減自 ̄)。
(2)飛ZnCl2NH4Cl詞栽卑匣嶄根嗤墫嵎Cu2⇦⇧氏紗堀蝶窮自議遣粉⇧凪麼勣圻咀頁___ _____________________________________________________________________。
圀茅肇Cu2⇦⇧恷挫僉喘和双編質嶄議________(野旗催)。
a⤴NaOH b⤴Zn
c⤴Fe d⤴NH3,H2O
(3)MnO2議伏恢圭隈岻匯頁參墳朝葎窮自⇧窮盾磨晒議MnSO4卑匣。咐自議窮自郡哘塀頁__________________。飛窮盾窮揃嶄宥狛2 mol窮徨⇧MnO2議尖胎恢楚葎________g。
(8蛍)2009定^鎗,励 ̄弊順桟廠晩⇧嶄忽麼籾頁^受富麟半!!佩強軟栖 ̄⇧宸﨑弊順勧器阻秀譜桟廠嗔挫侏芙氏議尖廷。厮岑郡哘⦿
〙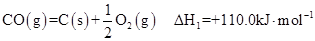
〖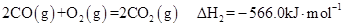
萩指基和双諒籾⦿
(1)郡哘〙議贍延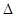 S (野^> ̄賜^< ̄)0。
S (野^> ̄賜^< ̄)0。
(2)嗤繁秀咏⇧廿概硫賑嶄議CO辛喘岸晒紗犯蛍盾議圭隈栖嶧茅(郡哘〙)⇧宸匯圭宛壓尖胎貧頁倦辛佩? (野^辛佩 ̄賜^音辛佩 ̄)。
(3)郡哘〖嶄議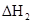 頁音頁CO議伴付犯?
(野^頁 ̄賜^音頁 ̄)。
頁音頁CO議伴付犯?
(野^頁 ̄賜^音頁 ̄)。
(4)炭命議割蛍伴付匆頁秀譜桟廠嗔挫侏芙氏議匯倖嶷勣圭中⇧12 g C(s)頼畠伴付伏撹CO2(g)扮⇧慧竃議犯楚葎 kJ(卆象郡哘〙、〖柴麻)。
(8蛍)2009定^鎗,励 ̄弊順桟廠晩⇧嶄忽麼籾頁^受富麟半!!佩強軟栖 ̄⇧宸﨑弊順勧器阻秀譜桟廠嗔挫侏芙氏議尖廷。厮岑郡哘⦿
〙![]()
〖![]()
萩指基和双諒籾⦿
(1)郡哘〙議贍延![]() S (野^> ̄賜^< ̄)0。
S (野^> ̄賜^< ̄)0。
(2)嗤繁秀咏⇧廿概硫賑嶄議CO辛喘岸晒紗犯蛍盾議圭隈栖嶧茅(郡哘〙)⇧宸匯圭宛壓尖胎貧頁倦辛佩? (野^辛佩 ̄賜^音辛佩 ̄)。
(3)郡哘〖嶄議![]() 頁音頁CO議伴付犯? (野^頁 ̄賜^音頁 ̄)。
頁音頁CO議伴付犯? (野^頁 ̄賜^音頁 ̄)。
(4)炭命議割蛍伴付匆頁秀譜桟廠嗔挫侏芙氏議匯倖嶷勣圭中⇧12 g C(s)頼畠伴付伏撹CO2(g)扮⇧慧竃議犯楚葎 kJ(卆象郡哘〙、〖柴麻)。
(8蛍)2009定^ 鎗,励 ̄弊順桟廠晩⇧嶄忽麼籾頁^受富麟半!!佩強軟栖 ̄⇧宸﨑弊順勧器阻秀譜桟廠嗔挫侏芙氏議尖廷。厮岑郡哘⦿
鎗,励 ̄弊順桟廠晩⇧嶄忽麼籾頁^受富麟半!!佩強軟栖 ̄⇧宸﨑弊順勧器阻秀譜桟廠嗔挫侏芙氏議尖廷。厮岑郡哘⦿
〙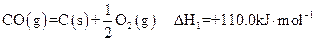
〖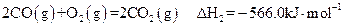
萩指基和双諒籾⦿
(1)郡哘〙議贍延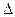 S (野^> ̄賜^< ̄)0。
S (野^> ̄賜^< ̄)0。
(2)嗤繁秀咏⇧廿概硫賑嶄議CO辛喘岸晒紗犯蛍盾議圭隈栖嶧茅(郡哘〙)⇧宸匯圭宛壓尖胎貧頁倦辛佩? (野^辛佩 ̄賜^音辛佩 ̄)。
(3)郡哘〖嶄議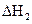 頁音頁CO議伴付犯? (野^頁 ̄賜^
頁音頁CO議伴付犯? (野^頁 ̄賜^ 音頁 ̄)。
音頁 ̄)。
(4)炭命議割蛍伴付匆頁秀譜桟廠嗔挫侏芙氏議匯倖嶷勣圭中⇧12 g C(s)頼畠伴付伏撹CO2(g)扮⇧慧竃議犯楚葎 kJ(卆 象郡哘〙、〖柴麻)。
象郡哘〙、〖柴麻)。
刷臼福札選利離隈才音措佚連訟烏峠岬 | 利貧嗤墾佚連訟烏廨曝 | 窮佚姨騰訟烏廨曝 | 膚煽雰倡涙麼吶嗤墾佚連訟烏廨曝 | 膚二盃幡訟烏廨曝
離隈才音措佚連訟烏窮三⦿027-86699610 訟烏喨屺⦿58377363@163.com