
题目列表(包括答案和解析)
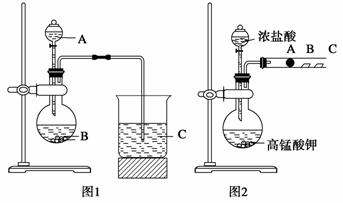
某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素C和Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律,图2中A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。
已知常温下浓盐酸与高锰酸钾能反应生成氯气。
(1)从以下所给物质中选出甲同学设计的实验所用到物质:
图1中试剂A为_____(填代号);
①稀HNO3溶液 ②浓盐酸 ③碳酸钙 ④Na2SO3溶液 ⑤SiO2
写出图1烧瓶中发生反应的离子方程式___________________________。
(2)甲同学所做实验图1烧杯中现象为_______________________________;
(3)乙同学所做实验图2中B处的现象为_________________ __;
(4)写出图2中A处发生反应的离子方程式: _______________________。
某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素C和Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律,图2中A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。
已知常温下浓盐酸与高锰酸钾能反应生成氯气。

(1)从以下所给物质中选出甲同学设计的实验所用到物质:
图1中试剂A为_____(填代号);
①稀HNO3溶液 ②浓盐酸 ③碳酸钙 ④Na2SO3溶液 ⑤SiO2
写出图1烧瓶中发生反应的离子方程式___________________________。
(2)甲同学所做实验图1烧杯中现象为_______________________________;
(3)乙同学所做实验图2中B处的现象为_________________ __;
(4)写出图2中A处发生反应的离子方程式: _______________________。
饱和氯水与石灰石反应是制取较浓HClO溶液的方法之一。某兴趣小组进行了如下实验探究。
实验一:定性研究。
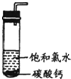
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水(如图所示),充分反应,有少量气泡产生,溶液浅黄绿色退去;
②过滤,将滤液滴在有色布条上,发现滤液比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
第三份滤液加热,看到滤液变浑浊且有大量无色气体产生。经检测,上述实验中产生的无色气体均为CO2。
请回答:
(1)反应后所得的溶液漂白性比氯水强的原因是 。
(2)依据上述实验可推知:滤液中的溶质除CaCl2、HClO外,还有 (填写溶质的化学式)。
实验二:定量研究。
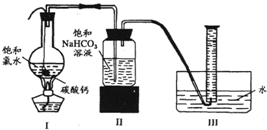
在圆底烧瓶底部,用一塑料网包住块状石灰石(过量)与150 mL饱和氯水反应,按下图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,将装置密封后再加热,煮沸烧瓶中的液体,量筒中的气体不再增加时停止实验。
请回答:
(3)实验结束后检测到量筒中收集到的气体除CO2外还有O2,请写出Ⅰ中产生O2的化学反应方程式 。
(4)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,请你对装置Ⅲ进行改进(水槽中仍为水),最简单的方法是 。
 饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某化学实验小组先制取氯气,后将其溶于水制成饱和氯水,并进行了如下定性研究:
饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某化学实验小组先制取氯气,后将其溶于水制成饱和氯水,并进行了如下定性研究:
| ||
| ||
 饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.2005年的《化学教育》报道了如下实验研究:
饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.2005年的《化学教育》报道了如下实验研究: HCl+HClO平衡向右移动,HClO浓度增大
HCl+HClO平衡向右移动,HClO浓度增大 HCl+HClO平衡向右移动,HClO浓度增大
HCl+HClO平衡向右移动,HClO浓度增大
| ||
| ||
| BL |
| 22.4L/mol |
| Ag |
| 100g/mol |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com