
题目列表(包括答案和解析)
0.1mol某烃在氧气中完全燃烧,将生成物全部通入浓硫酸中,浓硫酸增重9g,继续通入足量的澄清石灰水中,得到沉淀50g.
求:(1)该有机化合物的分子式
(2)若分子中只有两个甲基且属于不饱和烃,写出其结构简式
【解析】考查有机物分子式和结构式的判断。浓硫酸增重9g,说明生成物水是9g,物质的量是0.5mol。沉淀是碳酸钙,物质的量是0.5mol,则二氧化碳也是0.5mol。根据原子守恒可知分子式为C5H10。若属于不饱和烃,则是烯烃,分子中只有两个甲基,所以可能的结构简式是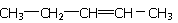 、
、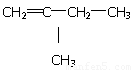 、
、 。
。
(11分)某溶液仅含下表离子中的5种(不考虑水的电离及离子的水解)且各种离子物质的量均为1mol。
阳离子:Na+ Mg2+ Fe3+ Al3+ Fe2+
阴离子:OH- CO32- Cl- NO3- SO42-
①若向溶液中加入KSCN溶液无明显变化;
②若向原溶液中加入稀盐酸,有无色气体生成,溶液中阴离子种类不变;请推断:
(1)原溶液中含有阳离子:________;含有阴离子:__________;
(2)向原溶液中加入足量稀盐酸发生反应的离子方程式:______ ___ _ ;
(3)若向原溶液中加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为__________g。
【解析】①说明没有Fe3+。加入盐酸阴离子种类不变,所以溶液中不能含有CO32-和OH-。又因为生成无色气体,在所给的离子中只有通过硝酸根的还原才能生成NO,所以原溶液中一定含有NO3-。所以必须有还原性离子,即一定含有亚铁离子。因为物质的量均是1mol,且只有5种离子,所以若镁离子、钠离子和铝离子同时存在,或存在2种,都不能满足溶液呈电中性,所以三者只能含有一种,因此氯离子和SO42-必须同时存在。根据离子的浓度大小可以判断,镁离子存在,铝离子和钠离子不能存在。若加入足量的氢氧化钠溶液,最终生成的沉淀是氢氧化镁和氢氧化铁,灼烧得到氧化镁和氧化铁,根据原子守恒可知,质量是1mol×40g/mol+0.5mol×160g/mol=120g。
(9分)A、B、C、D是中学化学中常见的四种化合物,它们分别由两种元素组成.甲、乙、丙是单质,甲、丙、A、C、D常温下均为气体,B为液体.这些单质和化合物之间存在如下关系:
(1)写出下列物质的分子式:A_______ 甲_______、丙_______.
(2)写出单质甲跟化合物C反应,生成SO2和化合物B的化学方程式_____________.
(3)标准状况下将28L化合物A与足量的过氧化钠充分反应转移电子的数目为
(4)在密闭容器中,化合物B跟化合物D在高温下生成化合物A和单质丙的反应是可逆反应,其化学方程式为__________。
(5)化合物C的稳定性比化合物B (填强或弱)。
【解析】本题属于无机框图题,关键是寻找突破点。常见的液体是水,则B是水。单质和化合物反应生成SO2和水的反应,根据原子守恒可知甲应是氧气,C是H2S。单质和气态化合物反应生成另外一种气态化合物的,常见的是CO2和C的反应生成CO,因此A是CO2,D是CO,乙是C。CO在高温下和水蒸气反应又生成CO2和氢气,所以丙是氢气。
(1)(2)(4)略
(3)28LCO2的物质的量是![]() 。CO2和过氧化钠反应的方程式为2CO2+2Na2O2=2Na2CO3+O2↑,在反应中过氧化钠既是氧化剂也是还原剂,转移的电子是2,所以当消耗1.25mol是转移的电子数目为1.25NA。
。CO2和过氧化钠反应的方程式为2CO2+2Na2O2=2Na2CO3+O2↑,在反应中过氧化钠既是氧化剂也是还原剂,转移的电子是2,所以当消耗1.25mol是转移的电子数目为1.25NA。
(5)S的非金属性弱于O的,所以H2S的稳定性弱于H2O的。
(9分)A、B、C、D是中学化学中常见的四种化合物,它们分别由两种元素组成.甲、乙、丙是单质,甲、丙、A、C、D常温下均为气体,B为液体.这些单质和化合物之间存在如下关系:
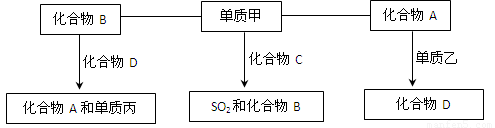
(1)写出下列物质的分子式:A_______ 甲_______、丙_______.
(2)写出单质甲跟化合物C反应,生成SO2和化合物B的化学方程式_____________.
(3)标准状况下将28L化合物A与足量的过氧化钠充分反应转移电子的数目为
(4)在密闭容器中,化合物B跟化合物D在高温下生成化合物A和单质丙的反应是可逆反应,其化学方程式为__________。
(5)化合物C的稳定性比化合物B (填强或弱)。
【解析】本题属于无机框图题,关键是寻找突破点。常见的液体是水,则B是水。单质和化合物反应生成SO2和水的反应,根据原子守恒可知甲应是氧气,C是H2S。单质和气态化合物反应生成另外一种气态化合物的,常见的是CO2和C的反应生成CO,因此A是CO2,D是CO,乙是C。CO在高温下和水蒸气反应又生成CO2和氢气,所以丙是氢气。
(1)(2)(4)略
(3)28LCO2的物质的量是 。CO2和过氧化钠反应的方程式为2CO2+2Na2O2=2Na2CO3+O2↑,在反应中过氧化钠既是氧化剂也是还原剂,转移的电子是2,所以当消耗1.25mol是转移的电子数目为1.25NA。
。CO2和过氧化钠反应的方程式为2CO2+2Na2O2=2Na2CO3+O2↑,在反应中过氧化钠既是氧化剂也是还原剂,转移的电子是2,所以当消耗1.25mol是转移的电子数目为1.25NA。
(5)S的非金属性弱于O的,所以H2S的稳定性弱于H2O的。
0.1mol某烃在氧气中完全燃烧,将生成物全部通入浓硫酸中,浓硫酸增重9g,继续通入足量的澄清石灰水中,得到沉淀50g.
求:(1)该有机化合物的分子式
(2)若分子中只有两个甲基且属于不饱和烃,写出其结构简式
【解析】考查有机物分子式和结构式的判断。浓硫酸增重9g,说明生成物水是9g,物质的量是0.5mol。沉淀是碳酸钙,物质的量是0.5mol,则二氧化碳也是0.5mol。根据原子守恒可知分子式为C5H10。若属于不饱和烃,则是烯烃,分子中只有两个甲基,所以可能的结构简式是、
、
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com