
题目列表(包括答案和解析)
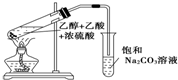
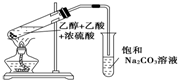 实验室用如图所示的装置制取乙酸乙酯
实验室用如图所示的装置制取乙酸乙酯

(15分)“旺旺雪饼”袋内有一个小纸袋,上面写着“干燥剂,主要成分是生石灰”。为此我对干燥剂的有关问题进行相关探究:
(1)问题1:为什么生石灰(CaO)可作干燥剂?(用化学方程式表示) 。
(2)我又对它作了一系列探究,获得较多收益,其有关实验方案如下:
|
问题与猜想 |
实验步骤 |
实验现象 |
实验结论 |
|
问题2:小纸袋中的物质 能否继续作干燥剂? |
取足量小纸袋中固体放入烧杯中,加入适量水,触摸杯壁。 |
|
不能作 干燥剂 |
|
问题3:我猜想变质后的物质可能是碳酸钙,该如何验证我的猜想? |
|
|
该干燥剂样品中有碳酸钙 |
(3)问题4:样品中碳酸钙的含量如何?某同学按如下流程进行实验:用盐酸溶解该干燥剂样品→干燥所得气体→用NaOH溶液吸收气体→根据NaOH溶液的增重计算该样品的含量,实验过程中所取该干燥剂样品的质量为10.0g。
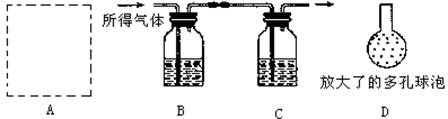
实验装置如图所示:
 .
.
①A为溶解该干燥剂样品的装置,若已准备了长颈漏斗、双孔橡胶塞、导气管,为完成溶解至少还需要的实验仪器是 。
②A中发生反应的化学方程式为
③将插入溶液C中管子的下端改成具有多孔的球泡(如图中的D),有利于提高实验的准确度,其理由是 。
④当改进实验装置并进行正确操作后可以准确测定出干燥剂样品的含量(假设生成气体没有损失,并完全吸收)。若此时C装置在实验前后其质量增加了3.6g,则该干燥剂样品的含量为 %。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com