
题目列表(包括答案和解析)
某课外活动小组在实验室用下图所示的装置进行实验,验证氨的某些性质并收集少量纯净氮气。试回答:
(1)实验前先将仪器按图连接好,然后 ,再开始实验。

(2)实验进行一段时间后,可以观察到硬质试管内黑色的CuO粉末变成
色,盛无水CuSO4的干燥管内出现 色,并在最后的出气导管处收集到纯净、干燥的N2。根据这些现象,硬质试管中的反应方程式为 ,这个反应说明氨气其有 性。
(3)烧瓶内盛有生石灰,随着浓氨水的滴入,产生氨气,氨气产生的原因是 。
(4)洗气瓶中浓硫酸的主要作用是 。
(5)在最后出气管口收集干燥、纯净的氮气,收集方法是 (填编号)
A.排气法 B.排水法 C.用塑料袋或球胆收集
纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数。
图中:①空气②某溶液③纯碱④某溶液⑤碱石灰(注:碱石灰既能吸收CO2,又能吸收H2O)
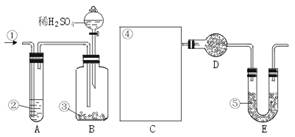 其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g)。c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为m2 g)。
其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g)。c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为m2 g)。
根据上述实验回答下列问题:
(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是____________________ 。装置A中盛装的液体“2”应选用________________,装置A的作用是________________,如果撤去装置A,直接向B中缓缓鼓入空气,则会导致实验测定结果(填“偏大”“偏小”或“不变”)________________。
(2)在空白格内画出装置C及试剂④是__________ ;装置C的作用是________________;如果撤去装置C,则会导致测定结果________________(填“偏大”“偏小”或“不变”)
(3)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________________(用m1、m2、n表示)
(4)装置E的作用是________________________。
纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数。图中:①空气②某溶液③纯碱④某溶液⑤碱石灰(注:碱石灰既能吸收CO2,又能吸收H2O)
其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g)。c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为m2 g)。根据上述实验回答下列问题:

(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是____________________ 。装置A中盛装的液体“2”应选用________________,
(2)在空白格内画出装置C及试剂④是______ ____ ;如果撤去装置C,则会导致测定结果________________(填“偏大”“偏小”或“不变”)
(3)装置E的作用是________________________
(4)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________________(用m1、m2、n表示)
纯碱中常含有少量的NaCl等杂质,利用下图仪器装置可用来测定纯碱中Na2CO3的质量分数.

图中:①空气,②某溶液,③纯碱,④稀H2SO4,⑥碱石灰.
其实验步骤是:
a.按上图所示,组装好实验仪器,并检查其气密性;
b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g);
c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内;
d.从分液漏斗中缓缓滴入一定量稀硫酸,并从①处缓缓鼓入空气,至B反应器中不再产生气体为止;
e.准确称量干燥管D的总质量(设为m2 g).
根据上述实验,回答下列问题:
(1)该实验进行至操作d时,要缓缓鼓入空气,鼓入空气的作用是________.装置A中盛装的液体②应选用________,装置A的作用是________,如果撤去装置A,直接向装置B中缓缓鼓入空气,则会导致实验测定结果________(填“偏大”、“偏小”或“不变”).
(2)在空白格内画出装置C及试剂,装置C盛放的试剂⑤是________,装置C的作用是________,如果撤去装置C,则会导致实验测定结果________(填“偏大”、“偏小”或“不变”).
(3)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________(用m1、m2、n表示).
(4)装置E的作用是________.
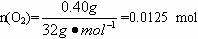
①按图装配实验装置。
②洗净试管然后充分干燥。
③向连接500 mL烧瓶和烧杯的玻璃管A、橡皮管B和玻璃管C中也装满水,在中间不要留下气泡,然后用弹簧夹把橡皮管B夹紧。
④称得试管的质量为14.45 g,往试管里加入KClO3和MnO2的混合物,再称其质量为15.95 g。
⑤打开弹簧夹,把烧杯举起使烧瓶、烧杯中的水面一致,再关闭弹簧夹,然后把烧杯中的水倒掉。
⑥打开弹簧夹,加热试管里的混合物到不再产生气体,即水不再流向烧杯时为止。
⑦反应完毕后把装置放置冷却到室温。
⑧调节烧杯的高度使烧杯中的水面一致,然后再关闭弹簧夹。
⑨用500 mL量筒测量烧杯里水的体积为285.0 mL,把它换算为标准状况下氧气的体积为279.7 mL。
⑩再称量冷却后试管的质量为15.55 g。
根据上述实验,完成下列问题。
(1)在操作①中,装置冷却后,玻璃管C的出口,一直要在烧杯的水中,不能离开水面,其理由是__________________________________。
(2)简述操作⑧的必要性,即为什么要调节烧杯的高度使烧杯中的水与烧瓶中的水面一致?
答:__________________________________________。
(3)标准状况下,1 mol氧气所占的体积(保留小数点后两位)为____________L;混合物中MnO2的质量分数为____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com