ÓÉHCl¡¢MgCl2¡¢AlCl3×é³ÉµÄ»ìºÏÈÜÒº1.0L£¬ÆäÖÐc(HCl)=0.1mol/L£¬c(MgCl2)=0.1mol/L£¬c(AlCl3)=1.2mol/L¡£
(1)ÒÑÖªÈÜÒºÖÐc(Mg2+)ÓëÈÜÒºµÄpHµÄ¹ØϵΪlgc(Mg2+)=17-2¡ÁpH£¬Ïò»ìºÏÈÜÒºÖмÓÈëNaOH¹ÌÌåÖÁpH=9£¬ÊÇ·ñÓÐMg(OH)2³ÁµíÉú³É£¿_____£¨Ìî¡°ÊÇ¡±»ò¡°·ñ¡±£©£¨²»¿¼ÂÇNaOHµÄ¼ÓÈëÒýÆðµÄÌå»ý±ä»¯£¬ÏÂͬ£©£¬ÔÒòÊÇ_____________________
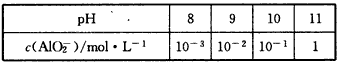
(2)Ïò»ìºÏÈÜÒºÖмÓÈëNaOH¹ÌÌ壬ÈÜÒºÖÐc(AlO2-)ËæpHµÄ±ä»¯ÈçÏ£º
ÊÔд³öÔÚ¼îÐÔÌõ¼þÏ£¬c(AlO2-)ÓëpHµÄ¹Øϵʽ£º_____________________
(3)Ïò»ìºÏÈÜÒºÖмÓÈëNaOH¹ÌÌåÖÁpH=11£¬ÐèÒªNaOHµÄÖÊÁ¿Îª¶àÉÙ£¿£¨µ±ÈÜÒºÖÐijÀë×ÓµÄŨ¶È¡Ü1¡Á10-5mol/Lʱ£¬¿ÉÊÓΪ¸ÃÀë×ÓÍêÈ«³Áµí£©£¨Ð´³ö¼ÆËã¹ý³Ì£©