
题目列表(包括答案和解析)
(10 分)

硫酸铜是一种用途广泛的化工原料。将适量稀硝酸分多次加人到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶,得到硫酸铜晶体(装置如图所示)。
(1)图中烧瓶内发生的离子反应方程式为:________________
(2)反应时B瓶内的现象是___________________________
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
把 作催化剂加人到铜粉与稀硫酸的混合物中,并通人空气或氧气,即发生反应。反应完全后向其中加人物质甲调节
作催化剂加人到铜粉与稀硫酸的混合物中,并通人空气或氧气,即发生反应。反应完全后向其中加人物质甲调节 ,产生
,产生 沉淀,过滤、蒸发、结晶,得到硫酸铜晶体,滤渣作催化剂循环使用。
沉淀,过滤、蒸发、结晶,得到硫酸铜晶体,滤渣作催化剂循环使用。
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使 分别生成沉淀的pH如下:
分别生成沉淀的pH如下:
|
物质 |
开始沉淀时的PH |
完全沉淀时的PH |
|
Fe(OH)3 |
1.9 |
3. 2 |
|
Cu(OH)2 |
4. 7 |
6. 7 |
|
Fe(OH)2 |
6. 3 |
9. 7 |
请回答下列问题:
①物质甲 是_____ (填字母序号)。
a.
 b.
b. c.
c. d.
d.
②该方案中调节PH的范围是______ 。

(10 分)
硫酸铜是一种用途广泛的化工原料。将适量稀硝酸分多次加人到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶,得到硫酸铜晶体(装置如图所示)。
(1)图中烧瓶内发生的离子反应方程式为:________________
(2)反应时B瓶内的现象是___________________________
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
把作催化剂加人到铜粉与稀硫酸的混合物中,并通人空气或氧气,即发生反应。反应完全后向其中加人物质甲调节
,产生
沉淀,过滤、蒸发、结晶,得到硫酸铜晶体,滤渣作催化剂循环使用。
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使分别生成沉淀的pH如下:
| 物质 | 开始沉淀时的PH | 完全沉淀时的PH |
| Fe(OH)3 | 1.9 | 3. 2 |
| Cu(OH)2 | 4. 7 | 6. 7 |
| Fe(OH)2 | 6. 3 | 9. 7 |
请回答下列问题:
①物质甲 是_____ (填字母序号)。
a. b.
c.
d.
②该方案中调节PH的范围是______ 。
(10 分)
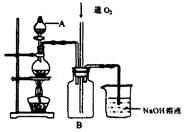
硫酸铜是一种用途广泛的化工原料。将适量稀硝酸分多次加人到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶,得到硫酸铜晶体(装置如图所示)。
(1)图中烧瓶内发生的离子反应方程式为:________________
(2)反应时B瓶内的现象是___________________________
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
把![]() 作催化剂加人到铜粉与稀硫酸的混合物中,并通人空气或氧气,即发生反应。反应完全后向其中加人物质甲调节
作催化剂加人到铜粉与稀硫酸的混合物中,并通人空气或氧气,即发生反应。反应完全后向其中加人物质甲调节![]() ,产生
,产生![]() 沉淀,过滤、蒸发、结晶,得到硫酸铜晶体,滤渣作催化剂循环使用。
沉淀,过滤、蒸发、结晶,得到硫酸铜晶体,滤渣作催化剂循环使用。
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使![]() 分别生成沉淀的pH如下:
分别生成沉淀的pH如下:
| 物质 | 开始沉淀时的PH | 完全沉淀时的PH |
| Fe(OH)3 | 1.9 | 3. 2 |
| Cu(OH)2 | 4. 7 | 6. 7 |
| Fe(OH)2 | 6. 3 | 9. 7 |
请回答下列问题:
①物质甲 是 (填字母序号)。
a. ![]() b.
b.![]() c.
c.![]() d.
d.![]()
②该方案中调节PH的范围是 。
 (2013?红桥区二模)为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.
(2013?红桥区二模)为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.
| ||
| ||
| 溶解度(S)/g | 溶度积(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
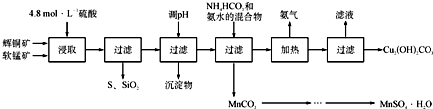
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe 3+ | 1.1 | 3.2 |
| Mn 2+ | 8.3 | 9.8 |
| Cu 2+ | 4.4 | 6.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com