
题目列表(包括答案和解析)
 在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.| 实验中可能出现的现象 | 结论 |
| 假设1成立 | |
| 假设2成立 | |
| 假设3成立 |
| 所选药品 | 有关化学方程式 |
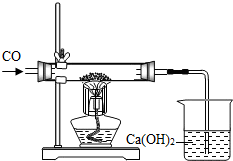 在实验课上,老师给了同学们一包红色的粉末,该粉末是铜粉和氧化铁中的一种或两种.同学们为了确定该粉末的成分,进行了如下探究.请你参与他们的探究并回答问题.
在实验课上,老师给了同学们一包红色的粉末,该粉末是铜粉和氧化铁中的一种或两种.同学们为了确定该粉末的成分,进行了如下探究.请你参与他们的探究并回答问题.| 实验中可能出现的现象 | 结论 |
红色粉末不变色,澄清石灰水不变浑浊 红色粉末不变色,澄清石灰水不变浑浊 |
假设1成立 |
红色粉末全部变黑色,澄清石灰水变浑浊 红色粉末全部变黑色,澄清石灰水变浑浊 |
假设2成立 |
红色粉末部分变黑色,澄清石灰水变浑浊 红色粉末部分变黑色,澄清石灰水变浑浊 |
假设3成立 |
| ||
| ||
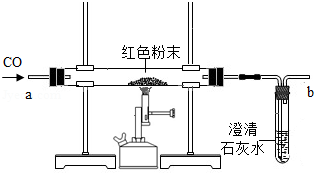
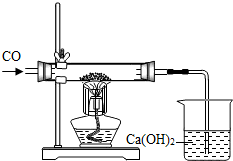 在实验课上,老师给了同学们一包红色的粉末,该粉末是铜粉和氧化铁中的一种或两种.同学们为了确定该粉末的成分,进行了如下探究.请你参与他们的探究并回答问题.
在实验课上,老师给了同学们一包红色的粉末,该粉末是铜粉和氧化铁中的一种或两种.同学们为了确定该粉末的成分,进行了如下探究.请你参与他们的探究并回答问题.| 实验中可能出现的现象 | 结论 |
| ________ | 假设1成立 |
| ________ | 假设2成立 |
| ________ | 假设3成立 |
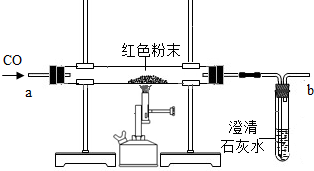 在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.| 实验中可能出现的现象 | 结论 |
| 假设1成立 | |
| 假设2成立 | |
| 假设3成立 |
| 所选药品 | 有关化学方程式 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com