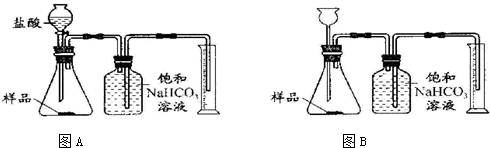
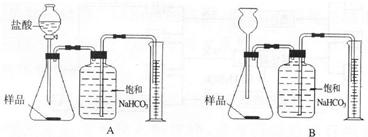
我国青海湖地区素有“夏天晒盐,冬天捞碱”之说,其中捞出的碱主要是碳酸钠和少量氯化钠的混合物.小王同学以捞出的碱作为样品,并用以下一套装置对样品进行分析,根据量筒中收集到的液体的体积(相当于二氧化碳的体积)来计算样品中碳酸钠的含量.(已知:HCl+NaHCO
3═NaCl+CO
2↑+H
2O;CO
2在饱和NaHCO
3溶液中溶解度很小)
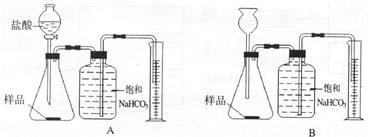
(1)在A和B 两套装置中,哪一套装置更合理
(选填“A”或“B”).
(2)准确读取量筒内液体体积的方法是
.
(3)锥形瓶中原有的空气对实验结果是否有明显影响?
(填“有”或“没有”).
(4)若实验中用的盐酸是浓盐酸,则测得的样品中碳酸钠的含量与实际值相比会
(填“偏大”或“偏小”或“不变”).
(5)在实验过程中,对取用样品的量的多少有一定要求,为什么?
.
(6)若取样品的质量为3g,反应停止后量筒内液体的体积为560mL(已知该条件下二氧化碳的密度为1.96g/L).试计算该样品中碳酸钠的含量(计算过程中保留两位小数).