
题目列表(包括答案和解析)
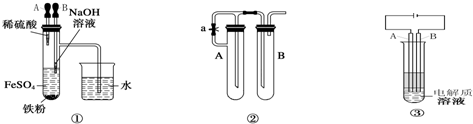
由于氢氧化亚铁在空气中能迅速被氧气氧化成氢氧化铁,因此要观察到氢氧化亚铁的颜色往往较为困难。某研究性学习小组的同学经过讨论后,设计出了三套能较长时间观察Fe(OH)2沉淀颜色的装置,如图。
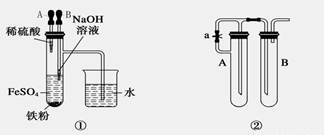
1.根据装置①,要想达到实验目的,应先挤胶头滴管_______(填“A”或“B”)
2.利用装置②,所用试剂为NaOH溶液、铁屑、稀硫酸,
(1)试管A中加入的试剂是_________试管B中加入的试剂是_______
(2)为了制得Fe(OH)2白色沉淀,现准备进行如下操作:先向试管A和B中加入试剂,然后_____(“打开”或“关闭”)止水夹,塞紧塞子,接下来的实验步骤是____________________
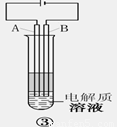
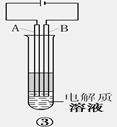
3.装置③时利用电解原理来达到实验目的的。
(1)电极材料是铁棒(Fe)和碳棒(C),A极应为_______(填材料的元素符号)
(2)电解质溶液可选用__________(填选项序号)
A.NaCl溶液 B.CuSO4溶液 C.Na2SO4溶液 D.NaOH溶液
(3)该实验准备选用一种有机物来起到隔绝空气的作用,该有机物可以是__________
由于氢氧化亚铁在空气中能迅速被氧气氧化成氢氧化铁,因此要观察到氢氧化亚铁的颜色往往较为困难。某研究性学习小组的同学经过讨论后,设计出了三套能较长时间观察Fe(OH)2沉淀颜色的装置,如图。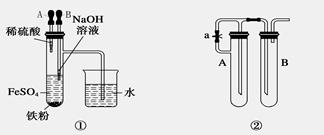
1.根据装置①,要想达到实验目的,应先挤胶头滴管_______(填“A”或“B”)
2.利用装置②,所用试剂为NaOH溶液、铁屑、稀硫酸,
(1)试管A中加入的试剂是_________试管B中加入的试剂是_______
(2)为了制得Fe(OH)2白色沉淀,现准备进行如下操作:先向试管A和B中加入试剂,然后_____(“打开”或“关闭”)止水夹,塞紧塞子,接下来的实验步骤是____________________
3.装置③时利用电解原理来达到实验目的的。
(1)电极材料是铁棒(Fe)和碳棒(C),A极应为_______(填材料的元素符号)
(2)电解质溶液可选用__________(填选项序号)
A.NaCl溶液 B.CuSO4溶液 C.Na2SO4溶液 D.NaOH溶液
(3)该实验准备选用一种有机物来起到隔绝空气的作用,该有机物可以是__________
Fe(OH)2是铁的一种氢氧化物,难溶于水,具有还原性,其制备方法较为特殊。下面是实验室制备
Fe(OH)2的方法之一:
(1)制备原理:利用复分解反应,使可溶性的亚铁盐溶液与可溶性的碱液反应生成Fe(OH)2。写出该反应的离子方程式_________________。
(2)NaOH溶液的制备:在试管中加入2~3 mL蒸馏水,加热至沸腾,冷却至室温,加入1片NaOH固体。制备NaOH溶液的蒸馏水加热的目的是___________。
(3)FeSO4溶液的制备:在试管中加入5 mL蒸馏水,并加热,直至蒸馏水沸腾,然后向蒸馏水中滴入几滴稀硫酸;待蒸馏水冷却至室温,加入少量FeSO4晶体,为了防止溶液中的Fe2+被氧化,在溶液中加入少量
____________。加入FeSO4晶体前在蒸馏水中加入稀硫酸的目的是____________。
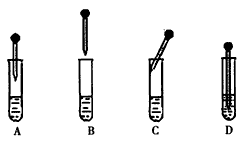
(4) Fe(OH)2的制备:下图中的胶头滴管中盛有NaOH溶液,试管中是FeSO4溶液。制备Fe(OH)2时正确的操作是___________(填字母序号),操作过程中________(填“能”或“不能”)振荡试管,原因是___________________。
(7分)二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下: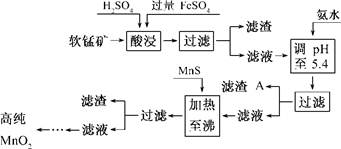
某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | pH |
| Al(OH)3 | 5.2 |
| Fe(OH)3 | 3.2 |
| Fe(OH)2 | 9.7 |
| Mn(OH)2 | 10.4 |
| Cu(OH)2 | 6.7 |
| Zn(OH)2 | 8.0 |
| CuS | ≥-0.42 |
| ZnS | ≥2.5 |
| MnS | ≥7 |
| FeS | ≥7 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com