
题目列表(包括答案和解析)
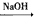 R-OH+HX(R表示烃基,X表 示卤原子);
R-OH+HX(R表示烃基,X表 示卤原子);
已知:①R―X+H2O ![]() R―OH+HX(R表示烃基,X表示卤原子);②有机物分子中的硝基可转变成氨基:R―NO2+Fe+HCl → R―NH2+FeCl2+H2O未配平)
R―OH+HX(R表示烃基,X表示卤原子);②有机物分子中的硝基可转变成氨基:R―NO2+Fe+HCl → R―NH2+FeCl2+H2O未配平)
“对乙酰胺基酚”俗称“扑热息痛”,为白色晶体,具有解热镇痛药效。扑热息痛的一种生产流程如下:

(1)写出反应②、⑤的化学方程式:
反应②: 。
反应⑤: 。
(2)有人认为上述流程反应②应当放在反应③后进行,你认为是否合理,说明理由:
。
(3)对扑热息痛的下列说法中正确的是(选填序号) 。
a.在溶液中1mol扑热息痛最多与1mol NaOH反应 b.能与溴水反应使溴水褪色
c.在其分子中含有肽键 d.遇氯化铁溶液发生显色反应
(4)写出与扑热息痛互为同分异构体,且分子中含有苯环的α―氨基酸的结构______。
| ||
| ||
| 操作步骤 | 预期现象和结论 |
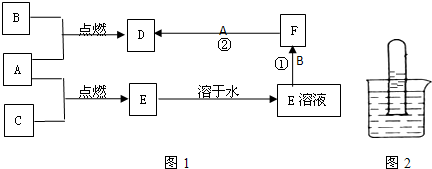
| 步骤1.取少量样品于试管中, 加入足量的3mol?L-1H2SO4,充分振荡 加入足量的3mol?L-1H2SO4,充分振荡 |
样品全部溶解 样品全部溶解 |
| 步骤2. 取少许溶液于试管中,加入足量铁粉,充分振荡;再加入足量3mol?L-1H2SO4,充分振荡 取少许溶液于试管中,加入足量铁粉,充分振荡;再加入足量3mol?L-1H2SO4,充分振荡 |
试管中出现红色固体,说明试样中有CuO 试管中出现红色固体,说明试样中有CuO |
| 36.5V |
| 22.4 |
| 36.5V |
| 22.4 |
| 36.5V |
| 22.4 |
| 36.5V |
| 22.4 |
| 22400 |
| 63.5 |
| 36.5V |
| 22.4 |
| 36.5V |
| 22.4 |
| 36.5V |
| 22.4 |
| 36.5V |
| 22.4 |
| 22400 |
| 63.5 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com