
题目列表(包括答案和解析)
 )与二苯酮反应制备三苯甲醇.
)与二苯酮反应制备三苯甲醇.

某研究性学习小组对过量炭粉与氧化铁反应中气体产物的成分进行了研究。
【提出假设】该反应中的气体产物可能是CO或者是CO2和CO的混合物。
【查阅资料】氮气不与碳、氧化铁发生反应。实验室可以用饱和氯化铵溶液和饱和亚硝酸钠(NaNO2)溶液混合加热反应制得氮气。
【设计方案】如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。

试回答下列问题:
(1)广口瓶内盛放的试剂为 ,其作用为
(2)实验开始时,应先打开弹簧夹,一段时间后关闭;再点燃酒精喷灯,理由是
(3)称取3.20g氧化铁、2.00g炭粉混合均匀,放入质量为48.48g的硬质玻璃管中;待反应结束,再通一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为51.24g。经进一步测定得知参加反应的氧元素质量为0.96g。从而确认该反应的气体产物是CO2和CO的混合物,理由是 。根据数据处理结果判断,反应产生的气体中n(CO2):n(CO)= 。
(4)有同学认为还应对该实验装置作进一步完善,你认为应作如何改进?
| ||
| ||

(8分)某化学兴趣小组在甲、乙两个充满氧气的密闭容器中各加入一定量的碳粉,在高温条件下使其充分反应,待反应结束后,两个容器中的碳粉都已完全消失。该小组成员对反应后两容器内气体进行如下探究:
⑴小红同学对甲容器中气体的组成提出如下四种猜想:
①只有CO ②只有CO2 ③只有O2 ④CO和O2的混合气体
你认为上述猜想中明显不合理的是 (填序号)
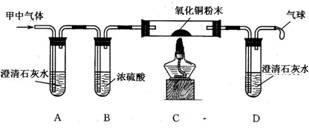
⑵小明同学认为甲容器中的气体还可能是CO和CO2的混合气体,为了验证自己的猜想,他准备按下图所示装置进行探究。
请你回答下列问题:
若小明的猜想成立,则装置A中反应的化学方程式是 ;装置C玻璃管中的实验现象是 ,反应的化学方程式是 。
⑶小芳同学对乙容器中气体的组成提出了除上述猜想外的另一种合理猜想,她的猜想是 ,于是她设计了下列实验方案验证其猜想:
【步骤1】先加热装有铜丝网的玻璃管一段时间后,再通入乙中的气体,观察现象;
【步骤2】将乙中的气体通入澄清石灰水,观察现象。
指导老师在分析其实验方案后,指出了其中存在的错误或不足。
①步骤1应先通入乙中气体一段时间后方可加热。你认为这样修改的原因是 。
②没有必要进行步骤2的实验,其理由是 。
⑷若反应前甲、乙两容器中碳粉与氧气的质量比分别表示为 (mC/mO2)甲
和(mC/mO2)乙,当小明和小芳的猜想均成立时,则(mC/mO2)甲__________
(mC/mO2)乙(填“﹥”、“﹤”或“=”)。
针对苏教版化学I第75页上“铁与氧化性较弱的氧化剂(如盐酸、硫酸铜溶液等)反应转化为+2价铁的化合物,如果与氧化性较强的氧化剂(如氯气、双氧水等)反应则转化为+3价的化合物”的叙述,化学研究性学习小组拟通过以下实验探究“新制的还原性铁粉和盐酸的反应(铁过量)”。请你参与探究并回答有关问题: (1)通过简单的化学实验检验反应后混合物中的二价铁的实验方法和现象是 ;但在实验中往往又看到血红色迅速褪去,同时溶液呈黄色,其可能的原因是: ;学生在做实验时往往滴加双氧水的浓度过大,或者过量,还看到迅速产生大量气泡,写出产生该现象的化学方
(1)通过简单的化学实验检验反应后混合物中的二价铁的实验方法和现象是 ;但在实验中往往又看到血红色迅速褪去,同时溶液呈黄色,其可能的原因是: ;学生在做实验时往往滴加双氧水的浓度过大,或者过量,还看到迅速产生大量气泡,写出产生该现象的化学方 程式: 。
程式: 。 (2)有资料介绍“取少量反应液(含二价铁)先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色。若再滴加过量新制氯水,却发现血红色褪去。同学对血红色褪去的原因提出各自的假
(2)有资料介绍“取少量反应液(含二价铁)先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色。若再滴加过量新制氯水,却发现血红色褪去。同学对血红色褪去的原因提出各自的假 设。某同学的假设是:溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式 。
设。某同学的假设是:溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式 。 (3)探究高铁酸钾的某种性质。
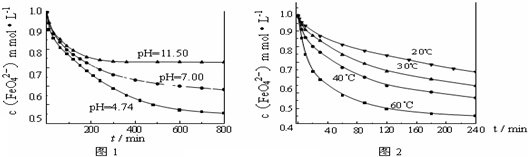
(3)探究高铁酸钾的某种性质。 【实验1】将适量K2FeO4固体分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0 mmol·L-1(1 mmol·L—1 =10—3 mol·L—1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。
【实验1】将适量K2FeO4固体分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0 mmol·L-1(1 mmol·L—1 =10—3 mol·L—1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。

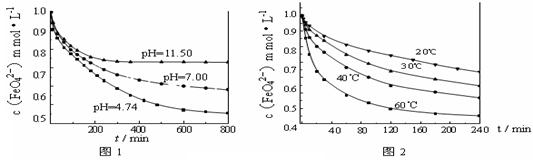

 【实验2】将适量 K2FeO4溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0 mmol·L-1的试样,将试样分别置于 20℃、30℃、40℃和60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则
【实验2】将适量 K2FeO4溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0 mmol·L-1的试样,将试样分别置于 20℃、30℃、40℃和60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则 ①实验1的目的是 ;
①实验1的目的是 ; ②实验2可得出的结论是 ;
②实验2可得出的结论是 ; ③高铁酸钾在水
③高铁酸钾在水 中的反应为4 FeO42—+10 H2O
中的反应为4 FeO42—+10 H2O 4 Fe(OH)3+8OH—+3 O2↑。由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是 。
4 Fe(OH)3+8OH—+3 O2↑。由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com