
题目列表(包括答案和解析)
下列关于接触法制硫酸的叙述中,不正确的是
[ ]
A.黄铁矿矿粒在沸腾炉内燃烧快,反应完全,提高了原料的利用率
B.炉气净化的目的是防止催化剂中毒
C.热交换器的目的是使 的热量传递给
的热量传递给 ,有利于
,有利于 的氧化和
的氧化和 的吸收
的吸收
D.吸收塔用水吸收 ,因为
,因为 在水中溶解度大,吸收完全
在水中溶解度大,吸收完全
下列关于接触法制硫酸的叙述中,不正确的是
[ ]
A.黄铁矿矿粒在沸腾炉内燃烧快,反应完全,提高了原料的利用率
B.炉气净化的目的是防止催化剂中毒
C.热交换器的目的是使 的热量传递给
的热量传递给 ,有利于
,有利于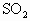 的氧化和
的氧化和 的吸收
的吸收
D.吸收塔用水吸收 ,因为
,因为 在水中溶解度大,吸收完全
在水中溶解度大,吸收完全
A.黄铁矿的主要成分是FeS B.热交换的目的是充分利用反应热
C.用水吸收SO3使之成为硫酸 D.尾气中含有SO2,需作净化处理
Ⅰ以下是有关SO2、Cl2的性质实验.
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.
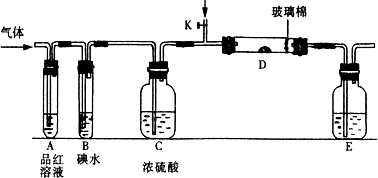
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?________(填“相同”或“不相同”);若装置D中装的是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为________.
②SO2通入B中,溶液颜色退去,则该反应的离子方程式为________.
(2)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母)________,仍然无法观察到沉淀产生.
A.氨水
B.稀盐酸
C.硝酸钾溶液
D.硫化钠溶液
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4∶3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式________.
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触.通入SO2的电极为________极,其电极反应式为________;电池的总反应式________

Ⅱ实验是化学研究的基础,关于下列各装置图的叙述正确的是________(填序号)
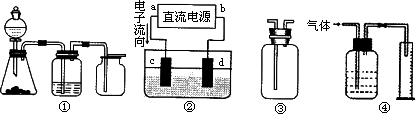
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正扳,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
D.装置④能用于测量气体体积
Ⅲ用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是________(填序号)
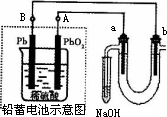
A.铅蓄电池负极的反应式为:Pb-2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com