
题目列表(包括答案和解析)
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等。
(1)对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物:
①CH4 (g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g) ΔH=-570 kJ·mol-1
②CH4(g)+4NO(g)="=2" N2(g) +CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
则CH4 (g)+2NO2(g)="=" N2(g)+CO2(g)+2H2O(g) ΔH=___________。
(2)将燃煤废气中的CO2转化为甲醚的反应原理为:2CO2(g)+6H2(g)  CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
已知在压强为a MPa下,该反应在不同温度、不同投料比时,CO2的转化率见下图: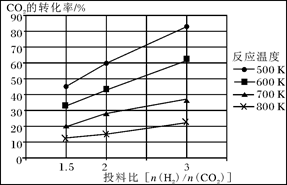
①此反应为 (填“放热”、“吸热”);若温度不变,提高投料比[n(H2)/n(CO2)],则K将________(填“增大”、“减小”或“不变”)。
②若用甲醚作为燃料电池的原料,请写出在碱性介质中电池正极的电极反应式_______________________。
③在a MPa和一定温度下,将6 mol H2和2 mol CO2在2 L密闭容器中混合,当该反应达到平衡时,测得平衡混合气中CH3OCH3的体积分数约为16.7%(即1/6),此时CO2的转化率是多少?(计算结果保留2位有效数字)
④在a MPa和500K下,将10mol H2和5 mol CO2在2 L密闭容器中混合,5min达到平衡,请在答题卡的坐标图中画出H2浓度变化图。(请标出相应的数据)
| |||||||||||||||||||||||||
理化性质:
又名亚硫酸酐(1),无色有强烈辛辣刺激味的不燃性气体。相对分子质量64.07,密度
职业接触:
燃烧含硫燃料(3)、熔炼硫化矿石、烧制硫磺、制造硫酸和亚硫酸、硫化橡胶、制冷(4)、漂白(5)、消毒(6)、熏蒸杀虫、镁冶炼、石油精炼、某些有机合成等作业工人和有关人员皆有可能接触。另外,它是常见的工业废气及大气污染的成分(7)。
毒性:
属中等毒类,对眼和呼吸道有强烈刺激作用(8),吸入高浓度二氧化硫可引起喉水肿、肺水肿、声带水肿及痉挛导致窒息。
根据以上文字内容完成(1)—(7)小题。
(1)亚硫酐是亚硫酸酸酐的简称。无机酸的酸酐是一种氧化物,其中非氧元素在氧化物中的化合价与该元素在酸中的化合价相同。据此判断下列各组合不是酸酐及其对应的酸的是( )
A.SO3 H2SO4 B.CO2 H2CO
(2)文中(2)处所述的反应的化学方程式为_______________________________ ;这两个反应的反应类型可描述为_________________。
A.化合反应 化合反应 B.化合反应 氧化还原反应
C.氧化还原反应 化合反应 D.氧化还原反应 氧化还原反应
(3)含硫燃料主要指( )
A.天然气 B.煤 C.石油 D.硫化氢气体
(4)二氧化硫用于制冷主要是因为二氧化硫( )
A.易被氧化 B.易溶于水 C.易液化 D.有毒
(5)下列物质能用二氧化硫漂白的是( )
A.石蕊溶液 B.溴水 C.品红溶液 D.酸性KMnO4溶液
(6)2003年春天我国人民团结奋斗,取得了抗击“非典型肺炎”的胜利。抗非过程中最重要的措施就是消毒。下列物质可以用于环境消毒的是( )
A.二氧化氯 B.过氧乙酸 C.“
(7)下列气体中不属于大气污染物的是( )
A.氯气 B.二氧化碳 C.二氧化硫 D.二氧化氮

(20分)A物质是实验室一种无色有毒的挥发性液体,由X、Y两种短周期元素组成。A在空气中极易着火生成B气体和C气体;A不溶于水,但加热到423K可以和水反应,生成B气体和D气体,D只含两种元素,其中一种是Y。在交流放电的情况下,分解生成E气体、F固体两种物质,E物质和B化学式量几乎相等,含Y元素约72.7%;F是环状单质分子,具有冠状结构,易溶于A,F的式量约是C的4倍。E可在液氮条件下与HBr于77K生成含双键结构的物质G,冷却至室温可得G的环状三聚体H。
6-1 写出A、B、C、D、E、F、G、H的结构简式。
6-2 用X射线衍射法测得F的晶体为正交晶系,晶胞参数a=1048pm,b=1292pm,c=2455pm。已知该物质的密度为2.07g?cm-3。计算每个晶胞中F分子的数目。
6-3 自发现富勒烯以来,其神奇的结构和性能引起了人们对碳原子团簇广泛和深入的研究。除了碳原子团簇之外,其它元素的原子团簇是否也具有类似碳原子团簇的奇异的特性,这是个十分有趣的研究课题。F物质有很多同分异构体,在实验手段受到各种条件的限制时,理论研究是一种重要的补充。厦门大学化学系对F物质的原子团簇进行了理论计算,发现除了冠状结构外还有多种结构。其中一种X具有2次对称轴,以及两个包含对称轴的对称面,一配位和三配位原子数目相等;另外一种Y是一种椅式结构原子团簇增加2个原子形成,也具有二次对称轴,对称面和对称轴垂直。请画出这两种结构的原子团簇。
6-4 五氟化砷AsF5(2.93g)和上述物质F(0.37g)用四氮化四硫S4N4(0.53g)在液态SO2溶剂中发生完全的反应,溶剂和挥发性产物被泵抽出后得黄色固体残留物L(3.08g),分析J知其含有:As 28.04%,F 42.70%,N 5.25%,经分析L是离子化合物,阴离子为正八面体结构,阳离子为两种元素组成,结构是直线形。固体L(0.48g)溶于液态二氧化硫,和叠氮化铯Cs+N3-(0.31g)完全反应,收集应释放出得氮气于66.5kPa、298K为67.1cm3。反应混合物过滤得难溶蓝黑色纤维状固体J(0.16g)。分析J知其含有2种元素,其中含N 30.3%。红外光谱、X射线粉末衍射结果表明抽出SO2后残留物是六氟砷(V)酸铯。
(1)L的实验式是什么?
(2)提出L的结构式;
(3)写出配平的生成L的方程式;
(4)1mol L发生转化时生成氮气的物质的量;
(5)J的化学式;
(6)写出n mol L生成J的普遍离子方程式。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com