
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)

(1)КөСйКТЦЖИЎ°ұЖшөД»ҜС§·ҪіМКҪОӘЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ¬№ӨТөЙПәПіЙ°ұІЙИЎөДПВБРҙлК©ЦРҝЙУГАХПДМШБРФӯАнҪвКНөДКЗ?ЎЎЎЎЎЎЎЎ?(МоЧЦДё)?
A.ІЙУГҪПёЯС№Зҝ(20 MpaЎ«50 Mpa)?
B.ІЙУГ500 ЎжөДёЯОВ?
C.УГМъҙҘГҪЧчҙЯ»ҜјБ?
D.Ҫ«ЙъіЙөД°ұТә»ҜІўј°КұҙУМеПөЦР·ЦАліцАҙЈ¬N2әНH2Сӯ»·өҪәПіЙЛюЦРІўІ№ідN2әНH2?
(2)ККөұёДұдИзНјЛщКҫөДЧ°ЦГәуЈ¬ТІҝЙУГАҙЦЖИЎәНКХјҜСхЖшЎЈёДұдөД·Ҫ·ЁКЗЈәЎЎЎЈ?
(3)КөСйКТУГЕЁБтЛбәННӯЦЖИЎІўКХјҜЙЩБҝөДSO2ЖшМеЈ¬ДЬ·сІЙУГёГЧ°ЦГЎЎ?ЎЎЎЎЎЎ?(МоЎ°ДЬЎұ»тЎ°І»ДЬЎұ)Ј¬ИфСЎМоЎ°ДЬЎұЈ¬ЗлЛөГчАнУЙЈ»ИфСЎМоЎ°І»ДЬЎұЈ¬ФтФхСщёДұдёГЧ°ЦГәуҫНДЬҙпөҪКөСйДҝөДЈҝЗлУГОДЧЦЛөГчЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ»?
(4)ИЎ6.4 gНӯЖ¬әН12 mL 18.4 molЎӨL-1ЕЁБтЛб·ЕФЪФІөЧЙХЖҝЦР№ІИИЈ¬ЦұөҪ·ҙУҰНкұПЈ¬Чоәу·ўПЦЙХЖҝЦР»№УРНӯЖ¬КЈУаЈ¬ДіН¬С§ёщҫЭЛщС§өД»ҜС§ЦӘК¶ИПОӘ»№УРТ»¶ЁБҝөДБтЛбКЈУаЎЈПВБРТ©Ж·ДЬ№»УГАҙЦӨГч·ҙУҰҪбКшәуЙХЖҝЦРИ·КөУРУаЛбөДКЗ??ЎЎЎЎЎЎЎЎ??(МоЧЦДё)ЎЈ?
A.Мъ·Ы B.ВИ»ҜұөИЬТә? C.Тш·Ы D.МјЛбЗвДЖИЬТә?
(5)ОӘ¶ЁБҝІв¶ЁУаЛбОпЦКөДБҝЕЁ¶ИЈ¬ДіН¬С§ҪшРРБЛИзПВЙијЖЈәПИІв¶ЁНӯЖ¬УлЕЁБтЛб·ҙУҰІъЙъSO2өДБҝЈ¬ФЩјЖЛгУаЛбөДОпЦКөДБҝЕЁ¶ИЎЈІв¶ЁSO2өДБҝөД·Ҫ°ёәЬ¶аЈ¬ПВБР·Ҫ°ёҝЙРРөД
КЗ (МоЧЦДё)?
A.Ҫ«Ч°ЦГЦРІъЙъөДЖшМе»ә»әНЁ№эФӨПИіЖБҝ№эКўУРјоКҜ»ТөДёЙФп№ЬЈ¬ҪбКш·ҙУҰәуФЩҙОіЖБҝ?
B.Ҫ«Ч°ЦГЦРІъЙъөДЖшМе»ә»әНЁИлЧгБҝЗвСх»ҜұөИЬТәЈ¬·ҙУҰНкИ«әу№эВЛЎўПҙөУЎўёЙІЩЎўіЖБҝіБөн?
C.Ҫ«Ч°ЦГЦРІъЙъөДЖшМе»ә»әНЁИлЧгБҝПхЛбЛб»ҜөДПхЛбұөИЬТәЈ¬·ҙУҰНкИ«әу№эВЛЎўПҙөУЎўёЙФпЎўіЖБҝіБөн?
Зл¶ФІ»ҝЙРРөД·Ҫ°ёҪшРР·ЦОц(ҝЙТФІ»МоВъ)
·Ҫ°ёРтәЕ | ·ЦОц | ОуІо(Ж«ёЯ»тЖ«өН) |
|
|
|
|
|
|
|
|
|
(6)ЗлФЩЙијЖЖдЛыҝЙРРөДКөСй·Ҫ°ёАҙІв¶ЁУаЛбөДОпЦКөДБҝЕЁ¶ИЈ¬јтТӘРҙіцІЩЧчІҪЦиј°РиТӘІв¶ЁөДКэҫЭ(І»ұШјЖЛг)ЎЈ??
| |||||||||||||||
КөСйКТНЁіЈУГЕЁБтЛбәНТТҙј·ҙУҰАҙЦЖИЎТТП©Ј¬іЈТтОВ¶И№эёЯ¶шЙъіЙЙЩБҝөД¶юСх»ҜБтЈ®УРИЛЙијЖПВБРКөСйТФИ·ИПЙПКц»мәПЖшМеЦРУРТТП©әН¶юСх»ҜБтЈ¬ўЪЧ°ЦГЦРДЬ·сКў·ЕдеЛ®Јҝ
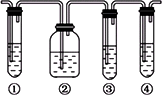
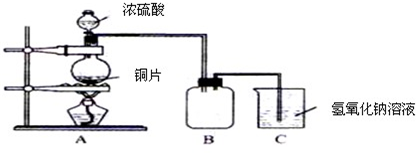
| ||
| ||
 N2+2CO2 Ҫ«УРәҰөДОЫИҫОпЧӘ»ҜОӘҝЙІОУлҙуЖшСӯ»·өДN2әНCO2Ј®
N2+2CO2 Ҫ«УРәҰөДОЫИҫОпЧӘ»ҜОӘҝЙІОУлҙуЖшСӯ»·өДN2әНCO2Ј®| Кұјд/h | 0 | 1 | 2 | 3 | 4 | 5 |
| cЈЁNOЈ©/mol?L-1 | 1.00ЎБ10-3 | 4.5ЎБ10-4 | 2.5ЎБ10-4 | 1.5ЎБ10-4 | 1.00ЎБ10-4 | 1.00ЎБ10-4 |
| cЈЁCOЈ©/mol?L-1 | 3.6ЎБ10-3 | 3.05ЎБ10-3 | 2.85ЎБ10-3 | 2.75ЎБ10-3 | 2.70ЎБ10-3 | 2.70ЎБ10-3 |
| ||
| ||
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com