
题目列表(包括答案和解析)
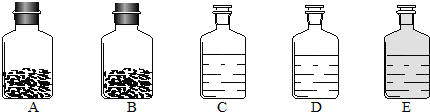
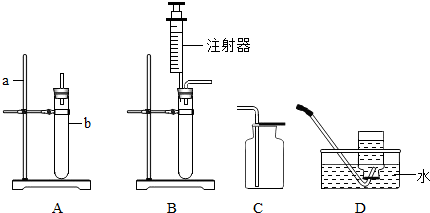
结合下列实验装置图回答问题:

(1)写出仪器的名称①________ ②________
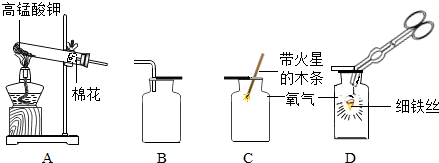
(2)实验室选用装置A作为制取氧气的发生装置,发生反应的文字表达式为________,反应的类型为________反应.收集氧气可选用E装置,理由是________,若选择C装置收集氧气,则验满的方法是________.用氯酸钾制氧气的实验中,如果发现试管破裂,原因可能是________.
(3)实验室选用装置B作为制取氧气的发生装置,发生反应的文字表达式为________,某同学在观察到锥形瓶内有大量气泡时,开始用C装置收集O2,过一段时间后,用带火星的木条身入瓶口、瓶中、瓶底,都没见木条复燃,其原因可能是________.若实验时用此法代替KMnO4加热制取O2,优点是________(填编号).
①生成物只有氧气
②不需加热
③需加热
(4)若装置B中反应很剧烈,据此提出实验安全注意事项是________(填编号)
①控制液体的加入速度
②用体积较小的锥形瓶
③加热反应物
(5)氨气极易溶于水,且密度比空气小,实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,发生装置应选用________装置,若使用装置H收集氨气,则气体应从________(填e或f)通入.
(6)F装置可以收集和储备氧气,若用水将装置中的氧气排出,水应从________端通入.
(7)利用药品氯酸钾和装置A、F(装满水)、G可以制取氧气并测量其体积,则接口的顺序为(填abcd):a→________→________→________,已知完全分解1.225克氯酸钾可以制取336 ml的氧气,实验结束后,测得量筒中水的体积为504.0 ml,则至少需要氯酸钾的质量为________(准确到2位小数).(以上数据均为标准状况下测得)
(8)通过两个月的化学学习,你应知道还有多种途径可以制得氧气.如:
A.电解水
B.分离空气
C.加热氧化汞
D.加热高锰酸钾等
请写出方法D制取氧气的文字表达式________.
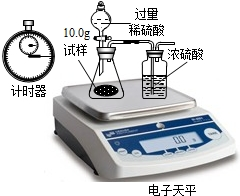
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.30 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 248.20 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 248.00 |

| 实验 序号 |
过氧化氢 溶液浓度∕% |
过氧化氢 溶液体积∕mL |
温度∕℃ | 二氧化锰 的用量∕g |
收集氧气 的体积∕mL |
反应所需的时间∕s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | ----------- | 2 | 49.21 |
| ④ | 30 | 5 | 55 | ----------- | 2 | 10.76 |



| 实验 序号 | 过氧化氢 溶液浓度∕% | 过氧化氢 溶液体积∕mL | 温度∕℃ | 二氧化锰 的用量∕g | 收集氧气 的体积∕mL | 反应所需的时间∕s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | ----------- | 2 | 49.21 |
| ④ | 30 | 5 | 55 | ----------- | 2 | 10.76 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com