
题目列表(包括答案和解析)
| ||
铁元素及其化合物与人类的生产生活息息相关,试回答下列问题:
(1)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,该反应的离子方程式为 。
(2)已知:Fe(s)+ O2(g)
O2(g) FeO(s) △H=-272 kJ·mol-1
FeO(s) △H=-272 kJ·mol-1
C(s)+O2(g) CO2(g) △H=-393.5 kJ·mol-1
CO2(g) △H=-393.5 kJ·mol-1
2C(s)+O2(g) 2CO(g) △H=-221 kJ·mol-1
2CO(g) △H=-221 kJ·mol-1
则高炉炼铁过程中 FeO(s)+CO(g) Fe(s)+CO2(g) △H= 。
Fe(s)+CO2(g) △H= 。
(3)铁红(Fe2O3)是一种红色颜料。将一定量的铁红溶于160mL 5 mol·L-1盐酸中,再加入足量铁粉,待反应结束共收集到气体2.24L(标准状况),经检测溶液中无Fe3+,则参加反应的铁粉的质量为 。
(4)以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如下图所示,其中P端通入CO2。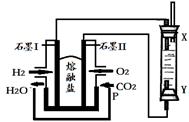
①石墨I电极上的电极反应式为 。
②通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是 (填序号)。
| A.X、Y两端都必须用铁作电极 |
| B.可以用NaOH溶液作为电解液 |
| C.阴极发生的反应是:2H2O+ 2e-= H2↑+ 2OH- |
| D.白色沉淀只能在阳极上产生 |
|
高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能净水的处理剂.工业制备高铁酸钾的离子反应方程式为:Fe(OH)3+ClO-+OH-→FeO42-+Cl-+H2O(未配平) 下列有关说法不正确的是 | |
| [ ] | |
A. |
由上述反应可知,Fe(OH)3的氧化性强于FeO42- |
B. |
高铁酸钾中铁显+6价 |
C. |
上述反应中氧化剂和还原剂的物质的量之比为3∶2 |
D. |
K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能净水的处理剂。工业制备高铁酸钾的离子反应方程式为:Fe(OH)3+ C1O—+ OH—→FeO42—+C1—+ H2O(未配平)
下列有关说法不正确的是( )
A.由上述反应可知,Fe(OH)3的氧化性强于FeO42—
B.高铁酸钾中铁显+6价
C.上述反应中氧化剂和还原剂的物质的量之比为3: 2
D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质
高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能净水的处理剂。工业制备高铁酸钾的离子反应方程式为:Fe(OH)3+ C1O—+ OH—→FeO42—+C1—+ H2O(未配平)
下列有关说法不正确的是( )
A.由上述反应可知,Fe(OH)3的氧化性强于FeO42—
B.高铁酸钾中铁显+6价
C.上述反应中氧化剂和还原剂的物质的量之比为3: 2
D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com