
题目列表(包括答案和解析)
(10分)在常温常压下,都用惰性材料作电极.分别电解(同浓度、同体积、通过相同电量)下列溶液:
| A.CuSO4 | B.AgNO3 | C.KOH | D.H2SO4 E.NaCl F.Na2SO4 |
(10分)如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹;x、y分别为直流电源的两极。在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入一多孔的惰性电极。切断电源开关S1,闭合开关S2,通直流电一段时间后,生成气体如图所示。
请回答下列问题:
(1)标出电源的正、负极:x为 。
(2)在滤纸的C端附近,观察到的现象是 。?
(3)写出电极反应式:B电极 。?
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2闭合开关S1,则电流计的指针是否发生偏转 (填“偏转”或“不偏转”)。?
(5)若电流计指针偏转,写出有关的电极反应(若指针“不偏转”,此题不必回答。);
。?
若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答) 。
(10分)如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹;x、y分别为直流电源的两极。在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入一多孔的惰性电极。切断电源开关S1,闭合开关S2,通直流电一段时间后,生成气体如图所示。
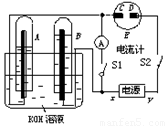
请回答下列问题:
(1)标出电源的正、负极:x为 。
(2)在滤纸的C端附近,观察到的现象是 。?
(3)写出电极反应式:B电极 。?
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2闭合开关S1,则电流计的指针是否发生偏转 (填“偏转”或“不偏转”)。?
(5)若电流计指针偏转,写出有关的电极反应(若指针“不偏转”,此题不必回答。);
。?
若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答) 。
A、B、C、D、E、F、G、H的转化关系如下图。已知A是一种盐,B、C为常见的金属。常温常压下D为无色无味气体,无色气体G遇空气变红棕色。用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液。

请回答下列问题:
(1)A的化学式为 。
(2)A溶液电解的化学方程式为 。
(3)E的稀溶液与F溶液反应的离子方程式 。
(4)电解400mL盐A的溶液一段时间后,断开电路,取出电极,测得所得到的气体D在标准状况下的体积为22.4mL,则电解后溶液的pH为 (假设溶液体积不变)。
(5)若向E的稀溶液中加入12.0g金属单质B和C的混合粉末,固体完全溶解,收集反应产生的气体,再向所得溶液中加入足量的氢氧化钠溶液,产生20.5g沉淀。则收集气体的物质的量是 。
 (2012?琼海一模)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属.通常条件下D、G为无色无味气体.已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液.各物质之间的转化关系如图(部分反应产物已略去).
(2012?琼海一模)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属.通常条件下D、G为无色无味气体.已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液.各物质之间的转化关系如图(部分反应产物已略去).湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com