
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
| ұаәЕ | СОЛб | NaOHИЬТә | Ўчt/Ўж |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |

| іЖ Бҝ По Дҝ | іЖ Бҝ Кұ јд | ЦКБҝЈЁgЈ© |
| КФСщ | 10.00 | |
| Ч°ЦГ+ПЎБтЛбЦКБҝ | 241.20 | |
| Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ | ·ҙУҰҝӘКјәу15Гл | 249.20 |
| Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ | ·ҙУҰҝӘКјәу35Гл | 249.00 |
| Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ | ·ҙУҰҝӘКјәу55Гл | 249.00 |
| ұаәЕ | СОЛб | NaOHИЬТә | Ўчt/Ўж |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
| іЖЎЎ БҝЎЎ ПоЎЎ Дҝ | іЖЎЎ БҝЎЎКұ јд | ЦКБҝЈЁgЈ© |
| КФСщ | 10.00 | |
| Ч°ЦГ+ПЎБтЛбЦКБҝ | 241.20 | |
| Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ | ·ҙУҰҝӘКјәу15Гл | 249.20 |
| Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ | ·ҙУҰҝӘКјәу35Гл | 249.00 |
| Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ | ·ҙУҰҝӘКјәу55Гл | 249.00 |
| ұаәЕ | СОЛб | NaOHИЬТә | Ўчt/Ўж |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |

| іЖ Бҝ По Дҝ | іЖ Бҝ Кұ јд | ЦКБҝЈЁgЈ© |
| КФСщ | 10.00 | |
| Ч°ЦГ+ПЎБтЛбЦКБҝ | 241.20 | |
| Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ | ·ҙУҰҝӘКјәу15Гл | 249.20 |
| Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ | ·ҙУҰҝӘКјәу35Гл | 249.00 |
| Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ | ·ҙУҰҝӘКјәу55Гл | 249.00 |
ЈЁ9·ЦЈ©ДіРЛИӨРЎЧйН¬С§ОӘЦӨГчNaOHИЬТәУлПЎСОЛб·ўЙъБЛЦРәН·ҙУҰЈ¬ҙУІ»Н¬ҪЗ¶ИЙијЖБЛИзПВКөСй·Ҫ°ёЈ¬ІўҪшРРКөСйЎЈ
IЎўКөСй·Ҫ°ё
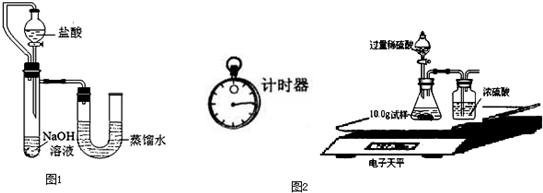
·Ҫ°ёТ»ЈәПИУГpHКФЦҪІв¶ЁNaOHИЬТәөДpHЈ¬ФЩөОјУСОЛбЈ¬ІўІ»¶ПХсөҙИЬТәЈ¬Н¬КұІв¶Ё»мәПИЬТәөДpHЈ¬ІвөГөДpHЦрҪҘұдРЎЦұөҪpHРЎУЪ7Ј¬ФтЦӨГчNaOHИЬТәУлПЎСОЛб·ўЙъБЛ»ҜС§·ҙУҰЎЈ
ўЕ·ҙУҰәуЈ¬ЛщөГИЬТәПФ РФ(МоЎ°ЛбЎұЎўЎ°јоЎұ»тЎ°ЦРЎұ)
ўЖУГpHКФЦҪІв¶ЁNaOHИЬТәpHКұЈ¬ХэИ·өДІЩЧчКЗЈә
ЎЈ
ўЗјтКцЗҝөчЎ°ІвөГөДpHРЎУЪ7ЎұөДАнУЙЈә
______________________________________________________________________________ЎЈ
·Ҫ°ё¶юЈә»ҜС§·ҙУҰЦРНЁіЈ°йЛжУРДЬБҝөДұд»ҜЈ¬ҝЙҪиЦъ·ҙУҰЗ°әуөДОВ¶Иұд»ҜАҙЕР¶П·ҙУҰөД·ўЙъЎЈИз№ыNaOHИЬТәУлПЎСОЛб»мәПЗ°әуОВ¶ИУРұд»ҜЈ¬ФтЦӨГч·ўЙъБЛ»ҜС§·ҙУҰЎЈ
ёГЧйН¬С§Ҫ«І»Н¬ЕЁ¶ИөДСОЛбәНNaOHИЬТәёч10 ҝЛ»мәПЈ¬УГОВ¶ИјЖІв¶ЁКТОВПВ»мәПЗ°әуОВ¶ИөДұд»ҜЈ¬ІўјЗВјБЛГҝҙО»мәПЗ°әуОВ¶ИөДЙэёЯЦөЎчtЈЁИзПВұнЈ©ЎЈ
|
ұаәЕ |
СОЛб |
NaOHИЬТә |
Ўчt/Ўж |
|
1 |
3.65©Ү |
2.00©Ү |
3.5 |
|
2 |
3.65©Ү |
4.00©Ү |
x |
|
3 |
7.30©Ү |
8.00©Ү |
14 |
ўИұнЦРx = ЎЈ
ўЙДіН¬С§ФЪГ»К№УГОВ¶ИјЖөДЗйҝцПВЈ¬НЁ№эПВНјЛщКҫЧ°ЦГНкіЙБЛКөСйЎЈФтёГН¬С§ёщҫЭКөСйПЦПуЈә
Ј¬ЕР¶ПNaOHИЬТәУлПЎСОЛб·ўЙъБЛЦРәН·ҙУҰЎЈ
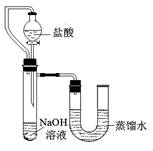
IIЎўКөСйЦРөДТвНвЗйҝц
ФЪКөСй№эіМЦРЈ¬ЛыГЗ·ўПЦКў·ЕNaOHИЬТәөДКФјБЖҝЖҝҝЪәНПрЖӨИыЙПіцПЦБЛ°ЧЙ«·ЫД©ЎЈЛыГЗТАҫЭЛщС§өД»ҜС§ЦӘК¶Ј¬¶ФХвЦЦ°ЧЙ«·ЫД©өДіЙ·ЦЧчБЛИзПВІВПлЈәўЩ ҝЙДЬКЗNaOHЈ»ўЪ ҝЙДЬКЗNa2CO3Ј» ўЫ ҝЙДЬКЗNaOHәНNa2CO3ЎЈ
ўКРЎГчН¬С§ИЎ°ЧЙ«·ЫД©ЙЩРнЈ¬ИЬУЪЛ®әуЈ¬ПИПтИЬТәЦРјУИлЧгБҝөД ИЬТәЈ¬ҝҙөҪ°ЧЙ«іБөнІъЙъЈ¬И»әуПтЙПІгЗеТәЦРјУИл·УМӘКФТәЈ¬ҝҙөҪИЬТәіКәмЙ«Ј¬СйЦӨБЛІВПлўЫКЗХэИ·өДЎЈ
ўЛОӘБЛҪшТ»ІҪСРҫҝЈ¬ИэО»Н¬С§ИЎБЛ10.0gЙПКцСщЖ·Ј¬АыУГөзЧУМмЖҪ№ІН¬ЧцБЛПВНјЛщКҫөДКөСйЎЈ

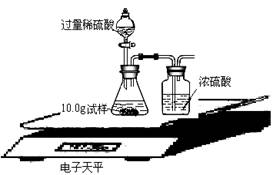
КөСйКэҫЭјЗВјИзПВЈә
|
іЖ Бҝ По Дҝ |
іЖ Бҝ Кұ јд |
ЦКБҝЈЁgЈ© |
|
КФСщ |
|
10.00 |
|
Ч°ЦГ+ПЎБтЛбЦКБҝ |
|
241.20 |
|
Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ |
·ҙУҰҝӘКјәу15Гл |
249.20 |
|
Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ |
·ҙУҰҝӘКјәу35Гл |
247.00 |
|
Ч°ЦГ+ПЎБтЛбЦКБҝ+КФСщ |
·ҙУҰҝӘКјәу55Гл |
247.00 |
КФНЁ№э·ЦОцұнЦРКэҫЭјЖЛгЙПКцСщЖ·ЦРёчіЙ·ЭөДЦКБҝ·ЦКэ·ЦұрКЗ¶аЙЩЈҝЈЁРҙіцјЖЛг№эіМЈ©ЎЈ
ЈЁ8Ј©УРН¬С§Мбіц°ҙЙПКцКөСйЛщІвөГКФСщЦРNa2CO3ЦКБҝ·ЦКэ»бЖ«РЎЈ¬ёГН¬С§өДАнУЙКЗЈЁКөСйІЩЧчҫщХэИ·Ј©Јә ЎЈ
| КөСйІҪЦи | КөСйПЦПу | Ҫб ВЫ |
| ўЩИЎ»мәПәуөД°ЧЙ«·ЫД©УЪКФ№ЬЦРЈ¬өОјУПЎСОЛбЈ¬Ҫ«ІъЙъөДЖшМеНЁИліОЗеөДКҜ»ТЛ®Ј® | УРЖшМеІъЙъ іОЗеөДКҜ»ТЛ®ұд»лЧЗ |
»мәПәуөД°ЧЙ«·ЫД©ЦРҝЙДЬУРЈә МјЛбДЖЎўМјЛбЗвДЖЎўМјЛбёЖ |
| ўЪИЎ»мәПәуөД°ЧЙ«·ЫД©УЪКФ№ЬЦРЈ¬јУЛ®ід·ЦИЬҪвЈ® | КФ№ЬөЧІҝУРДСИЬОпіцПЦЈ¬КФ№ЬНвұЪОЮГчПФұд»Ҝ |
»мәПәуөД°ЧЙ«·ЫД©ЦРТ»¶ЁУРЈә МјЛбёЖ Т»¶ЁГ»УРЈә ЗвСх»ҜДЖ |
| ўЫИЎІҪЦиўЪөДЙПІгЗеТәУЪКФ№ЬЦРЈ¬өОјУ·УМӘКФјБЈ® | ИЬТәұдіЙәмЙ« |
»мәПәуөД°ЧЙ«·ЫД©ЦР ҝЙДЬУРМјЛбДЖ»тМјЛбЗвДЖ |
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com