
题目列表(包括答案和解析)
| ||
| ||
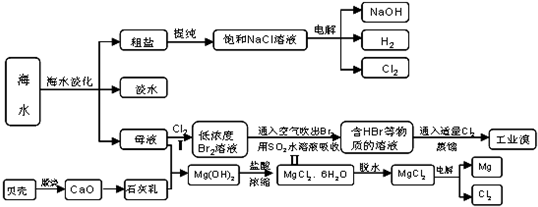
海水资源的利用将走综合开发的道路,一次提取海水,同时提取多种物质。下图是某工厂对海水资源综合利用的示意图。

试回答下列问题:
(1)提纯粗盐后的母液中含有K+、Mg2+、Na+等阳离子,对母液进行一系列的加工可以制得金属镁。
①从充分利用当地海洋化学资源,提高生产与经济效益的角度考虑,生产石灰乳的化学方程式是__________________________________________。
②从离子反应的角度思考,在母液中加入石灰乳的目的是____________________________;
③在生产中,常涉及反应MgCl2·6H2O![]() MgCl2+6H2O,该反应需要在HCl气氛中才能顺利完成,其理由是_______________________。
MgCl2+6H2O,该反应需要在HCl气氛中才能顺利完成,其理由是_______________________。
(2)在提取Mg(OH)2后和剩余母液中加入一种常见的气态氧化剂,又可制取重要的化工原料溴单质。
①生产中将溴单质从混合物中分离出来的方法是_________________。
②以下是对生产溴单质所用的气态氧化剂寻找提供货源的设想,其中合理的是___________。
A.从外地购买
B.从本厂生产烧碱处循环
C.从本厂生产镁单质处循环
D.在当地新建生产工厂
③从多种经营综合开发,打造大而强的现代化企业及本厂生产所需要的原料等方面来看,你认为该厂还可以再增加的生产项目是_________________。
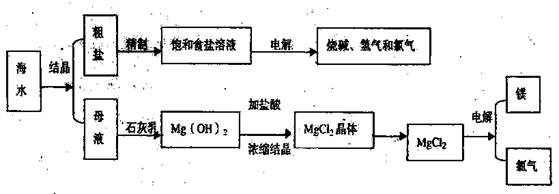
(12分)海水是取之不尽用之不竭的化学资源,从海水中可提取多种化工原料,下图是某化工厂对海水资源综合利用的示意图。
回答下列问题:
(1)请写出电解食盐水的离子方程式 。
(2)母液中含有K+、Na+、Mg2+等阳离子,从图中可看出对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是: 。
②石灰乳是生石灰与水作用形成的化合物,从充分利用当地海洋化学资源,提高生产与经济效益的角度考虑,生产生石灰的主要原料是 ;
③电解熔融氯化镁的化学方程式是 ;
④电解无水氯化镁所得的镁蒸气在特定的环境里冷却后可得固态的金属镁,下列物质中可用作镁蒸气的冷却剂是(填写代号) 。
A.H2 B.Cl2 C.空气 D.O2
E.水蒸气
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入一种常见的气态氧化剂,又制取了重要的化工原料溴单质:
①生成溴单质的化学反应的离子方程式是
②以下是对生产溴单质所用的气态氧化剂寻找货源的主凤想,其中合理的是
(填写代号)
A.以外地购买 B.在当地新建生产厂
C.从本厂生产烧碱外循环 D.从木厂生产镁单质处循环
③从各种经营综合开发,打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目是 。
(12分)海水是取之不尽用之不竭的化学资源,从海水中可提取多种化工原料,下图是某化工厂对海水资源综合利用的示意图。
回答下列问题:
(1)请写出电解食盐水的离子方程式 。
(2)母液中含有K+、Na+、Mg2+等阳离子,从图中可看出对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是: 。
②石灰乳是生石灰与水作用形成的化合物,从充分利用当地海洋化学资源,提高生产与经济效益的角度考虑,生产生石灰的主要原料是 ;
③电解熔融氯化镁的化学方程式是 ;
④电解无水氯化镁所得的镁蒸气在特定的环境里冷却后可得固态的金属镁,下列物质中可用作镁蒸气的冷却剂是(填写代号) 。
A.H2 B.Cl2 C.空气 D.O2
E.水蒸气
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入一种常见的气态氧化剂,又制取了重要的化工原料溴单质:
①生成溴单质的化学反应的离子方程式是
②以下是对生产溴单质所用的气态氧化剂寻找货源的主凤想,其中合理的是
(填写代号)
A.以外地购买 B.在当地新建生产厂
C.从本厂生产烧碱外循环 D.从木厂生产镁单质处循环
③从各种经营综合开发,打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目是 。
(12分)海水是取之不尽用之不竭的化学资源,从海水中可提取多种化工原料,下图是某化工厂对海水资源综合利用的示意图。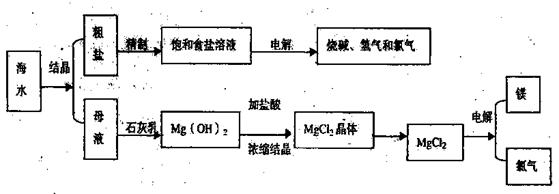
回答下列问题:
(1)请写出电解食盐水的离子方程式 。
(2)母液中含有K+、Na+、Mg2+等阳离子,从图中可看出对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是: 。
②石灰乳是生石灰与水作用形成的化合物,从充分利用当地海洋化学资源,提高生产与经济效益的角度考虑,生产生石灰的主要原料是 ;
③电解熔融氯化镁的化学方程式是 ;
④电解无水氯化镁所得的镁蒸气在特定的环境里冷却后可得固态的金属镁,下列物质中可用作镁蒸气的冷却剂是(填写代号) 。
A.H2 B.Cl2 C.空气 D.O2
E.水蒸气
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入一种常见的气态氧化剂,又制取了重要的化工原料溴单质:
①生成溴单质的化学反应的离子方程式是
②以下是对生产溴单质所用的气态氧化剂寻找货源的主凤想,其中合理的是
(填写代号)
A.以外地购买 B.在当地新建生产厂
C.从本厂生产烧碱外循环 D.从木厂生产镁单质处循环
③从各种经营综合开发,打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com