
题目列表(包括答案和解析)
2005年诺贝尔化学奖授予在发现有机物合成转换方面作出杰出贡献的三名科学家:法国的伊夫·肖万、美国的罗伯特·格拉布和理查德·施罗克。三位科学家获奖原因就是对有机化学烯烃复分解反应的研究作出贡献:反应机理可表示为: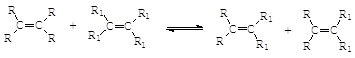
已知同温同压下,C相对于氢气的密度为14,I的分子式为C8H14O4,试根据下图关系,回答问题:
⑴已知C的燃烧热为Q kJ/mol,写出C完全燃烧的热化学方程式: 。
⑵化合物D、E、G、F中,具有羟基的是 。
⑶反应①、②、③、④、⑤中,属于加成反应的是 。
⑷写出A的结构简式: 。
⑸写出F+H→I反应的化学方程式: 。
⑹写出G发生银镜反应的化学方程式: 。
2005年诺贝尔化学奖授予在发现有机物合成转换方面作出杰出贡献的三名科学家:法国的伊夫·肖万、美国的罗伯特·格拉布和理查德·施罗克。三位科学家获奖原因就是对有机化学烯烃复分解反应的研究作出贡献:反应机理可表示为:
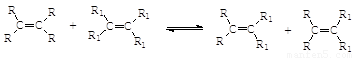
已知同温同压下,C相对于氢气的密度为14,I的分子式为C8H14O4,试根据下图关系,回答问题:

⑴已知C的燃烧热为Q kJ/mol,写出C完全燃烧的热化学方程式: 。
⑵化合物D、E、G、F中,具有羟基的是 。
⑶反应①、②、③、④、⑤中,属于加成反应的是 。
⑷写出A的结构简式: 。
⑸写出F+H→I反应的化学方程式: 。
⑹写出G发生银镜反应的化学方程式: 。


| |||||||||||||||||||||||
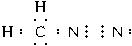
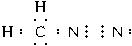
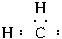
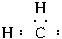
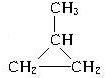

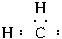 +CH3CH=CHCH3→
+CH3CH=CHCH3→
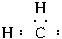 +CH3CH=CHCH3→
+CH3CH=CHCH3→
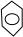 +
+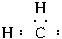 →
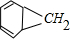
→
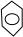 +
+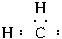 →
→
第Ⅰ卷(选择题,共63分)
一二.选择题。(3’×9+4’×9)
题号
1
2
3
4
5
6
7
8
9
答案
A
C
D
B
D
C
B
B
C
题号
10
11
12
13
14
15
16
17
18
答案
D
AC
B
AC
BC
B
C
CD
A
第Ⅱ卷(非选择题,共83分)
三.(本题包括3小题,共32分)
19.(9分)(1)双氧水(1分),Na2O2(其它合理答案也可)(1分)(2)a(1分)
(3)吸收多余氯气,防止污染空气。(2分)
(4)洗气瓶.安全瓶(其它合理答案也可)(各2分,共4分)
20.(11分)(1)固体完全溶解,溶液呈血红色(2分) (2)ABC(3分)
(3) Fe2O3+6H+===2Fe3++3H2O Cu2O+2H+===Cu+Cu2++H2O 2Fe3++Cu===2Fe2++Cu2+(每个离子方程式2分,共6分)
21.(12分)(1)B.锌粒(1分) C.水(1分) D.浓硫酸(1分)
(2)检查气密性(1分) 将G弯管浸没在盛有水的烧杯中,关闭分液漏斗活塞,温热烧瓶B,观察G管口,若有气泡逸出,停止加热后,G管倒吸形成一段水柱,说明装置的气密性良好(2分)(3)先从A瓶逐滴滴加液体(1分) 检验H2的纯度(1分)
(4)氢气(1分) 在G管出口处点燃(1分)
(5)
 或
或  (2分)
(2分)
四.(本题包括3小题,共31分)
22.(8分)(1)14HNO3+3Cu2O = 6Cu(NO3)2+2NO↑+7H2O。(2分) (2)酸性;氧化性(2分) (3)0.6 mol(2分) (4)使用了较浓的硝酸,产物中有部分二氧化氮生成。(2分)
 23.(14分)(1)2Na+2H2O=2Na++2OH-+H2↑ (2分) (2)酸(1分) NH4++H2O
23.(14分)(1)2Na+2H2O=2Na++2OH-+H2↑ (2分) (2)酸(1分) NH4++H2O NH3?H2O+H+ (2分)
(3)CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890.3KJ/mol (2分)
(4)I.NO2(2分)Ⅱ.b (1分) Ⅲ.0.8(或0.8mol/L) (2分) Ⅳ.增大NO2的浓度(合理均可)(2分)
NH3?H2O+H+ (2分)
(3)CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890.3KJ/mol (2分)
(4)I.NO2(2分)Ⅱ.b (1分) Ⅲ.0.8(或0.8mol/L) (2分) Ⅳ.增大NO2的浓度(合理均可)(2分)
24.(9分)(1)
(2)氧化.2Cl-+2e-=Cl2↑;
CaCl2+2H2O=Ca(OH)2+Cl2↑+H2↑;
(3)①F极放出黄绿色气体,E极放出无色气体;
②E极附近溶液变为红色;
③溶液变浑浊
五.(本题包括1小题,共10分)
25.(10分)29.(1) E F(2分)(2) ①③(2分)
 (3)A.CH3CH=CH2 ,
I.
(3)A.CH3CH=CH2 ,
I. 。(4分)
。(4分)
(4)(2分)
六.(本题包括2小题,共10分,任意选做一题,如果两道题都做,则按第26题给分)
26.⑴酯基.碳碳双键.苯环(3分)⑵加成(加聚)(2分)⑶(3分)
|