
题目列表(包括答案和解析)
SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如下图所示实验装置。

(1).检查该装置的气密性时,先在试管中装入适量的水(保证玻璃导管的下端浸没在水中),然后_______________________________________(填写操作方法)时,将会看到________________(填写实验现象),则证明该装置的气密性良好( )
A.向外轻轻拉动注射器的活塞 浸没在水中的玻璃导管口有气泡冒出
B.向内轻轻推动注射器的活塞 浸没在水中的玻璃导管口有气泡冒出
C.向外轻轻拉动注射器的活塞 浸没在水中的玻璃导管口有水柱上升
D.手握试管 浸没在水中的玻璃导管口有气泡冒出
(2).向试管中加入0.000 5 mol/L碘水1.0 mL,用适量的蒸馏水稀释后再加入2~3滴淀粉溶液,配制成溶液A。测定指定地点的空气中SO2的含量时,推拉注射器的活塞反复抽气,A溶液由________色变成______色时反应恰好完全进行,此时停止抽气( )
A.红 无 B.无 红 C.蓝 无 D.无 蓝
(3).我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值如下表:
|
浓度限值/mg/m3 |
||
|
一级标准 |
二极标准 |
三级标准 |
|
0.15 |
0.50 |
0.70 |
该学生课外活动小组分成第一小组和第二小组,使用相同的实验装置和溶液A。在同一地点、同时测量空气中SO2的含量。反应恰好完全进行,记录抽气次数和结果如下(假设每次抽气500 mL)。
|
分组 |
第一小组 |
第二小组 |
|
抽气次数 |
100 |
120 |
|
SO2含量/mg/m3 |
0.64 |
0.53 |
____小组的测定结果正确( )
A.第一 B.第二
C.都正确 D.都不正确
(4).判断该地点的空气中SO2的含量属于________标准( )
A.一级 B.二级 C.三级 D.四级
(5).实验结果产生较大偏差的原因是(所用装置和药品均无问题)( )
A.抽气速度过快,造成空气中SO2无法与碘水充分反应,产生较大的误差
B.抽气速度过慢,造成空气中SO2无法与碘水充分反应,产生较大的误差
C.装置漏气,造成空气中SO2无法与碘水充分反应,产生较大的误差
D.抽气速度过快,造成空气中O2与碘水充分反应,产生较大的误差
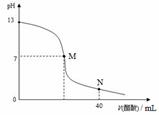
向20 mL NaOH溶液中逐滴加入0.1 mol/L醋酸溶液,滴定曲线如右图所示。下列判断正确的是( )

A.在M点,两者恰好反应完全
B.滴定前,酸中c(H+) 等于碱中c(OH-)
C.NaOH溶液的物质的量浓度为0.1 mol/L
D.在N点,c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH)
向20 mL NaOH溶液中逐滴加入0.1 mol/L醋酸溶液,
滴定曲线如右图所示。下列判断正确的是
A.在M点,两者恰好反应完全
B.滴定前,酸中c(H+) 等于碱中c(OH-)
C.NaOH溶液的物质的量浓度为0.1 mol/L
D.在N点,c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH)
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(用已被溶解的溶质的物质的量/
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)_______________(填“增大”“减小”或“不变”)。
(3)在
(4)由上述Ksp判断,在上述(3)的体系中,___________(填“能”或“否”)实现AgY向AgZ的转化,简述理由:_______________________________________________________。
(Ⅱ) “嫦娥一号”成功发射,实现了中国人的“奔月”梦想。
(1)发射“嫦娥一号”的长征三号甲火箭的第三级使用的推进剂是液氢和液氧,下列是298 K时,氢气(H2)、碳(C)、辛烷(C8H18)、甲烷(CH4)燃烧的热化学方程式:H2(g)+![]() O2(g)
O2(g)![]() H2O(l);ΔH=-285.8 kJ·mol
H2O(l);ΔH=-285.8 kJ·mol![]() CO2(g);ΔH=-393.5 kJ·mol
CO2(g);ΔH=-393.5 kJ·mol![]() O2(g)
O2(g)![]() 8CO2(g)+9H2O(l);ΔH=-5 518 kJ·mol-1 CH4(g)+2O2(g)
8CO2(g)+9H2O(l);ΔH=-5 518 kJ·mol-1 CH4(g)+2O2(g)![]() CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
通过计算说明等质量的H2、C、C8H18、CH4完全燃烧时,放出热量最多的是_____________,发射“嫦娥一号”的长征三号甲火箭的第三级使用液氢和液氧这种推进剂的优点是__________
__________________________;____________________________________。(请写两条)
(2)已知:H2(g)![]() H2(l);ΔH=-0.92 kJ·mol-1
H2(l);ΔH=-0.92 kJ·mol-1
O2(g)![]() O2(l);ΔH=-6.84 kJ·mol-1
O2(l);ΔH=-6.84 kJ·mol-1
H2O(l)![]() H2O(g);ΔH=44.0 kJ·mol-1
H2O(g);ΔH=44.0 kJ·mol-1
请写出液氢和液氧生成气态水的热化学方程式______________________________________。
如果此次发射“嫦娥一号”的长征三号甲火箭所携带的燃料为45吨,液氢、液氧恰好完全反应生成气态水,总共释放能量________kJ(保留3位有效数字)。
(3)氢气、氧气不仅燃烧时能释放热能,二者形成的原电池还能提供电能,美国的探月飞船“阿波罗号”使用的就是氢氧燃料电池,电解液为KOH溶液,其电池反应式为:负极:____________;正极:____________;总反应式:________________________。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com