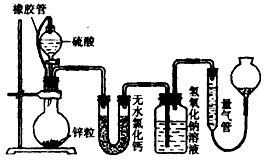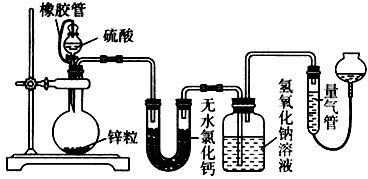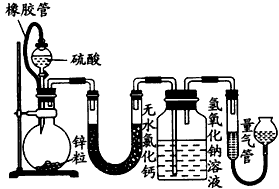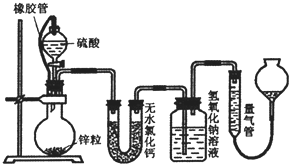
不同浓度的硫酸与锌反应时,硫酸可以被还原为S0
2,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.
(1)该小组设计了如图所示的实验装置,检查该装置气密性的操作是
.
(2)若在烧瓶中放入1.30g锌粒,与c mol?L
-1H
2SO
4,反应.为保证实验结论的可靠,量气管的适宜规格是(填字母)
A.100mL B.200mL C.400mL D.500mL
(3)若1.30g锌粒完全溶解.氢氧化钠洗气瓶增重0.64g(烧瓶中残留气体忽略不计,下同).则圆底烧瓶中发生反应的化学方程式为
.
(4)若烧瓶中投入a g锌且完全反应,氢氧化钠洗气瓶增重b g,量气管中收集到V mL气体(标准状况),请用一个代数式表示出a、b、V之间的关系
.
(5)若撤走盛有无水氯化钙的U型管,则n(H
2)/n(SO
2)的数值将
(填“偏大”、“偏小”或“无影响”).
(6)反应结束后,为了准确地测量气体体积,读数时应注意的事项是
、
.

 不同浓度的硫酸与锌反应时,硫酸可以被还原为S02,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.
不同浓度的硫酸与锌反应时,硫酸可以被还原为S02,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.