
题目列表(包括答案和解析)
某科学实验小组欲用如下图所示的实验装置来验证牺牲阳极的阴极保护法的原理.已知:
3Fe2++2Fe(CN)63-(黄色)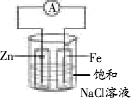
实验步骤如下:
[实验I]向100 mL烧杯中加入约50 mL饱和食盐水后,插入两个玻璃筒(无底).将一根锌棒和一根铁棒用导线与电流计连接后,再分别插入两个玻璃筒中,可以看到电流计指针发生偏转.
(1)电流计指针发生偏转的原因是________.锌棒上发生的反应为________,铁棒上发生的反应为________.
(2)可以证明该实验中无Fe2+产生的现象是________.
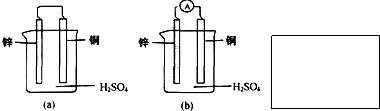
[实验II]为了进一步探究金属腐蚀的原理,该小组的同学又做了如下实验:
a.向100 mL烧杯中加入约50 mL饱和食盐水后,插入两个玻璃筒(无底);
b.将一根铜棒与一根铁棒用导线与电流计连接后,再分别插入两个玻璃筒中;
c.1 min后,向插入铁棒的玻璃筒内滴入2~3滴K3[Fe(CN)6]溶液;
d.向插入铜棒的玻璃筒内滴入酚酞溶液.
(3)b步骤中观察到电流计指针偏转但其偏转方向与实验I相反,表明________.
(4)c步骤中观察到的现象是________,表明________.
(5)d步骤中观察到的现象是________,表明________.
(6)通过上述实验可以得出的结论是________.
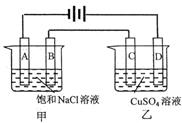 电解原理在化学工业上有着广泛的应用,按下图所示所示装置进行电解实验。A、B、C、D均为惰性电极,开始电解前在甲装置的A、B极两侧各滴入酚酞试液。
电解原理在化学工业上有着广泛的应用,按下图所示所示装置进行电解实验。A、B、C、D均为惰性电极,开始电解前在甲装置的A、B极两侧各滴入酚酞试液。
工作一段时间后:
(1)A极附近可观察到的现象是_____________________
_______________________________________________;
检验B电极上反应产物的通常方法是_____________;
甲电池中电解反应的离子方程式是 _______________________________________;
溶液中还可能存在的离子反应方程式是 ____________________________________。
(2)甲槽溶液的pH________________________(填“增大”、“不变”或 “减小”,下同);乙槽溶液的pH_______________。当A极上收集到22.4L气体(标准状况)时,乙装置的C极上可得到____________g金属单质。
利用A、D两极上析出的物质制成的燃料电池,是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答(3)~(6):
(3)氢氧燃料电池的能量转化主要形式是 ,
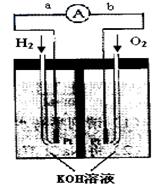 在导线中电子流动方向为 (用a、b 表示)。
在导线中电子流动方向为 (用a、b 表示)。
(4)负极反应式为 ____________。
(5)电极表面镀铂粉的原因为 __________
(6)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2=2LiH Ⅱ.LiH+H2O==LiOH+H2↑
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
②先用锂吸收224L(标准状况)H2,将生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
(15分)镁、铝是生活中两种常见的金属,课堂上老师演示了系列关于镁、铝性质的实验,某学习小组在组长的带领下进行归纳整理,并进行了深入的思考。
(1) “位置和结构”
①铝元素在周期表的位置是 镁原子电子式
(2) “基本性质”
②下列关于镁、铝及其化合物性质的说法,正确的是 (不定项选择)
A.镁在氯气中剧烈燃烧,产物中只有离子键
B.电解熔融的Al2O3可以制备金属铝
C.Al和MgO按照适当比列混合可做“铝热剂”,发生“铝热反应”
D.铝片放入冷的浓硝酸中,无明显现象,未发生化学反应
(3)设计实验验证“金属性:Mg > Al”
实验一:截取一段大小和形状相同的“经过一定预处理”的镁片和铝片,放入试管中,同时加入浓度和体积均相同的盐酸,观察某种实验现象,得到结论“金属性:Mg> Al”
③镁片和铝“经过一定预处理”,下列实验操作达到“预处理”效果的是
A.用砂纸打磨镁片和铝片
B.用盐酸浸泡镁片和铝片片刻
C.用烧碱溶液浸泡镁片和铝片片刻
④ 通过观察某种实验现象得到结论,该实验现象是
实验二:如右图,甲乙试管中分别加入2ml 1mol/L MgCl2和AlCl3溶液,用胶滴管逐滴滴加5mol/L NaOH溶液至过量。
⑤该“对照实验”甲、乙试管中分别出现实验现象能得出“金属性:Mg> Al”
甲试管现象
乙试管离子方程式
实验三:利用原电池原理也可得出“金属性:Mg> Al”,
⑥请在右框中画出一个原电池装置图,能够通过观察实验现象判定金属性:Mg>Al
可用材料:镁片、铝片、导线,其它试剂和材料、仪器可自选。
(15分)镁、铝是生活中两种常见的金属,课堂上老师演示了系列关于镁、铝性质的实验,某学习小组在组长的带领下进行归纳整理,并进行了深入的思考。
(1) “位置和结构”
①铝元素在周期表的位置是 镁原子电子式
(2) “基本性质”
②下列关于镁、铝及其化合物性质的说法,正确的是 (不定项选择)
A.镁在氯气中剧烈燃烧,产物中只有离子键
B.电解熔融的Al2O3可以制备金属铝
C.Al和MgO按照适当比列混合可做“铝热剂”,发生“铝热反应”
D.铝片放入冷的浓硝酸中,无明显现象,未发生化学反应
(3)设计实验验证“金属性:Mg > Al”
实验一:截取一段大小和形状相同的“经过一定预处理”的镁片和铝片,放入试管中,同时加入浓度和体积均相同的盐酸,观察某种实验现象,得到结论“金属性:Mg > Al”
③镁片和铝“经过一定预处理”,下列实验操作达到“预处理”效果的是
A.用砂纸打磨镁片和铝片
B.用盐酸浸泡镁片和铝片片刻
C.用烧碱溶液浸泡镁片和铝片片刻
④通过观察某种实验现象得到结论,该实验现象是
实验二:如右图,甲乙试管中分别加入2ml 1mol/L MgCl2和AlCl3溶液,用胶滴管逐滴滴加5mol/L NaOH溶液至过量。
⑤该“对照实验”甲、乙试管中分别出现实验现象能得出“金属性:Mg > Al”
甲试管现象
乙试管离子方程式
实验三:利用原电池原理也可得出“金属性:Mg > Al”,
⑥请在右框中画出一个原电池装置图,能够通过观察实验现象判定金属性:Mg >Al
可用材料:镁片、铝片、导线,其它试剂和材料、仪器可自选。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com