
题目列表(包括答案和解析)
下列叙述中,正确的是
A、金属性越强,其最高价氧化物对应水化物的碱性越强
B、金属性越强,等物质的量单质与足量的酸反应生成的氢气越多
C、金属性越强,其单质晶体的熔点越高
D、金属性越强,其对应的阳离子的氧化性越强
下列叙述中,正确的是
| A.金属性越强,其最高价氧化物对应水化物的碱性越强 |
| B.金属性越强,等物质的量单质与足量的酸反应生成的氢气越多 |
| C.金属性越强,其单质晶体的熔点越高 |
| D.金属性越强,其对应的阳离子的氧化性越强 |
| A.金属性越强,其最高价氧化物对应水化物的碱性越强 |
| B.金属性越强,等物质的量单质与足量的酸反应生成的氢气越多 |
| C.金属性越强,其单质晶体的熔点越高 |
| D.金属性越强,其对应的阳离子的氧化性越强 |
用“>”或“<”回答下列问题:
(1)酸性: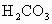 _______
_______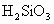 ,
,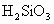 ________
________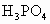
(2)碱性: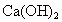 ________
________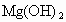 ,
,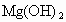 ________
________
(3)气态氢化物稳定性: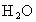 ________
________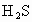 ,
,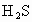 ________HCl
________HCl
(4)还原性: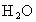 ________
________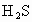 ,
,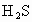 ________HCl
________HCl
(5)酸性: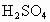 ________
________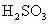 ,
,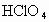 ________HClO
________HClO
从以上答案中可以归纳出:
(1)元素的非金属性越强,其对应最高价氧化物水化物的酸性越________.
(2)元素的金属性越强,其对应最高价氧化物水化物的碱性越________.
(3)元素的________性越强,其对应气态氢化物的稳定性越________.
(4)非金属性越强的元素生成的气态氢化物,其还原性越________.
(5)同种非金属性元素形成的含氧酸,其成酸元素价态越高,其酸性也越________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com