
题目列表(包括答案和解析)
温度 压强/Pa 平衡浓度/mol×L-1
25℃ 1´105 1.0
25℃ 2´105 1.8
25℃ 4´105 3.2
25℃ 5´105 6.0
(1)可逆反应中系数n的取值范围为_______,理由_______。
(2)在5´105Pa时,D的状态为_______。
常温常压下,A、B、C、D均为气态。A与B可发生可逆反应:A+BƒC+nD。若将2mol A和2mol B混合充入体积可变的密闭容器中,在不同条件下达平衡时C的浓度如下:
温度 压强/Pa 平衡浓度/mol×L-1
25℃ 1´105 1.0
25℃ 2´105 1.8
25℃ 4´105 3.2
25℃ 5´105 6.0
(1)可逆反应中系数n的取值范围为_______,理由_______。
(2)在5´105Pa时,D的状态为_______。
(2003年上海高考题)钾是一种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取。该反应为:Na(l)+KCl(l)![]() NaCl(l)+K(g)(正反应为吸热反应),各物质的沸点与压强的关系见下表。
NaCl(l)+K(g)(正反应为吸热反应),各物质的沸点与压强的关系见下表。
压强(kPa) 13.33 53.32 101.3
K的沸点(℃) 590 710 770
Na的沸点(℃) 700 830 890
KCl的沸点(℃) 1437
NaCl的沸点(℃) 1465
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为________,而反应的最高温度应低于_______
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是________。
压强(kPa) 13.33 53.32 101.3
K的沸点(℃) 590 710 770
Na的沸点(℃) 700 830 890
KCl的沸点(℃) 1437
NaCl的沸点(℃) 1465
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为________,而反应的最高温度应低于_______
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是________。
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:(将配平后的系数填在横线上)
__ C+ __ KMnO4+ ___ H2SO4→___CO2↑+ ___MnSO4 + ___K2SO4+ ___H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) ![]() CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
①实验1中以v (CO2)表示的反应速率为 (取小数二位,下同)。
②该反应为 (填“吸”或“放”)热反应,实验2条件下平衡常数K= 。
(3)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH =-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH =-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH =-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式
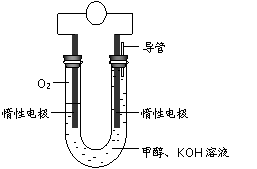 |
⑷某实验小组依据甲醇燃烧的反应原理,设计如右图所示的电池装置。
①该电池正极的电极反应为 。
②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为 。
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10—9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10—4mo1/L ,则生成沉淀所需CaCl2溶液的最小浓度为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com