
题目列表(包括答案和解析)
1932年,美国化学大师Linus Pauling提出电负性(用希腊字母χ表示)的概念,用来确定化合物中原子某种能力的相对大小.Linus Pauling假定F的电负性为4,并通过热化学方法建立了其他元素的电负性.Linus Pauling建立的主族元素的电负性如下:
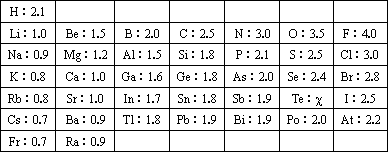
请仔细分析,回答下列问题:
(1)你认为Linus Pauling提出电负性的概念是确定化合物中原子哪种能力的相对大小?________________;
(2)预测Te元素χ的值________;
(3)根据表中所给数据分析研究推测:
同主族的不同元素的电负性变化的规律是________________,同周期中,电负性与原子半径的关系为________________________.
(4)一般认为,当两种成键元素的电负性差值小于1.7时,这两种元素通常形成共价化合物.根据H和F的电负性差值能否判断HF是离子化合物,并说明理由:________________________________.
(5)2005年1月美国科学家在《Science》上发表论文,宣布发现了Al的超原子结构Al13和Al14,并预言其它金属原子也可能存在类似的结构.这种超原子具有40个价电子(价电子即最外层电子)时最稳定.请预测Al14与周期表中________族元素的性质相似.
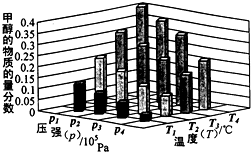 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚. 乙二胺四乙酸(EDTA)及其盐是常用于定量检测和分析金属离子的重要试剂.EDTA的阴离子可简写为Y4-,它与一些金属离子反应生成稳定的金属有机化合物离子:M2++Y4-=(MY)2-;M3++Y4-=(MY)-.
乙二胺四乙酸(EDTA)及其盐是常用于定量检测和分析金属离子的重要试剂.EDTA的阴离子可简写为Y4-,它与一些金属离子反应生成稳定的金属有机化合物离子:M2++Y4-=(MY)2-;M3++Y4-=(MY)-.| M2+ | K[(MY)2-] | Ksp(MS) | 填“是”或“否” |
| Pb2+ | 2×1018 | 4×10-26 | |
| Cd2+ | 2.6×1016 | 1×10-20 |
| C((CdY) 2-) |
| c(Cd2+)×c(Y4-) |
| 0.01-x |
| x×(0.49+x) |
| 0.01 |
| 0.49x |
| C((CdY) 2-) |
| c(Cd2+)×c(Y4-) |
| 0.01-x |
| x×(0.49+x) |
| 0.01 |
| 0.49x |
| M2+ | K[(MY)2-] | Ksp(MS) | 填“是”或“否” |
| Pb2+ | 2×1018 | 4×10-26 | |
| Cd2+ | 2.6×1016 | 1×10-20 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com