
题目列表(包括答案和解析)
某铜矿石中铜元素含量较低,且含有铁、镁、钙等杂质离子。某小组在实验室中用浸出-萃取法制备硫酸铜:
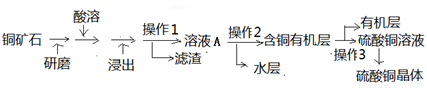
(1)操作1的名称为 。操作2用到的玻璃仪器有烧杯和
(2)“浸出”步骤中,为提高铜的浸出率,可采取的措施有
(3)比较操作2之前与操作3之后的溶液,说明两步骤主要目的是 。
(4)取少量所得溶液A,滴加 (填物质名称)溶液后呈红色,说明溶液中存在Fe3+,检验溶液中还存在Fe2+的方法是 (注明试剂、现象)(不考虑除注明外的其它杂质干扰)
(5)用滴定法测定CuSO4·5H2O的含量。取a g试样配成100 mL溶液,取20.00mL用c mol /L 滴定剂(H2Y2–,滴定剂不与杂质反应)滴定至终点,消耗滴定剂bmL.
滴定反应:Cu2+ +
H2Y2– CuY2–+
2H+。则CuSO4·5H2O质量分数的表达式是
。
CuY2–+
2H+。则CuSO4·5H2O质量分数的表达式是
。
(6)下列操作会导致CuSO4·5H2O含量的测定结果偏高的是_____________。
A.滴定临近终点时,用洗瓶中的蒸馏水洗下滴定管尖嘴口的半滴标准液至锥形瓶中
B.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00mL进行滴定
C.滴定前,滴定管尖端有气泡,滴定后气泡消失
某食用白醋是由醋酸与纯水配制而成,用0.1000 mol/L NaOH溶液准确测定其中醋酸的物质的量浓度。以下为某同学列出的实验步骤(未排序),请回答下列问题。
A.分别向碱式滴定管、酸式滴定管注入NaOH标准溶液和待测醋酸至0刻度以上2~3cm
B.调节滴定管液面至0或0刻度以下,记下读数
C.用NaOH标准溶液滴定至终点,记下滴定管液面的刻度
D.用标准溶液清洗碱式滴定管2~3次;待测醋酸清洗酸式滴定管2~3次
E.用待测醋酸清洗锥形瓶2~3次
F.排气泡使滴定管尖嘴充满溶液,把滴定管固定好
G.滴定管检漏,用水清洗所有仪器,备用
H.通过酸式滴定管向锥形瓶注入20.00 mL待测醋酸,并加入2-3滴指示剂
(1)用离子方程式表示该实验的原理 。
(2)从上述实验步骤中选出正确的并按操作先后排序。你的实验顺序为:(用字母
表示) 。
(3)实验室常用的酸碱指示剂有甲基橙、石蕊和酚酞,你选择的指示剂是________,
理由是_______________________________________________________________ ;
滴定终点的现象是______________________________________________________。
(4)某同学实验后得到的数据如下:
|
滴定次数 实验数据 |
1 |
2 |
3 |
4 |
5 |
|
V(NaOH) /mL(初读数) |
0.00 |
0.20 |
0.00 |
0.10 |
0.05 |
|
V(NaOH) /mL(终读数) |
15.75 |
15.20 |
14.98 |
15.12 |
15.05 |
原白醋中醋酸的物质的量浓度为____________mol/L(结果保留4位有效数字)。
(5)分析下列操作对测定结果的影响,用“偏低”、“偏高”或“不影响”填空。
①滴定前碱式滴定管充满溶液,滴定后尖嘴处有气泡_______;
②读取标准溶液体积时,滴定前平视,滴定后仰视________。
某铜矿石中铜元素含量较低,且含有铁、镁、钙等杂质离子。某小组在实验室中用浸出-萃取法制备硫酸铜:
(1)操作1的名称为 。操作2用到的玻璃仪器有烧杯和
(2)“浸出”步骤中,为提高铜的浸出率,可采取的措施有
(3)比较操作2之前与操作3之后的溶液,说明两步骤主要目的是 。
(4)取少量所得溶液A,滴加 (填物质名称)溶液后呈红色,说明溶液中存在Fe3+,检验溶液中还存在Fe2+的方法是 (注明试剂、现象)(不考虑除注明外的其它杂质干扰)
(5)用滴定法测定CuSO4·5H2O的含量。取a g试样配成100 mL溶液,取20.00mL用c mol /L 滴定剂(H2Y2–,滴定剂不与杂质反应)滴定至终点,消耗滴定剂bmL.
滴定反应:Cu2+ + H2Y2– CuY2–+ 2H+。则CuSO4·5H2O质量分数的表达式是 。
CuY2–+ 2H+。则CuSO4·5H2O质量分数的表达式是 。
(6)下列操作会导致CuSO4·5H2O含量的测定结果偏高的是_____________。
A.滴定临近终点时,用洗瓶中的蒸馏水洗下滴定管尖嘴口的半滴标准液至锥形瓶中
B.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00mL进行滴定
C.滴定前,滴定管尖端有气泡,滴定后气泡消失
某研究小组模拟工业上以黄铁矿为原料制备硫酸的第一步反应如下:
4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。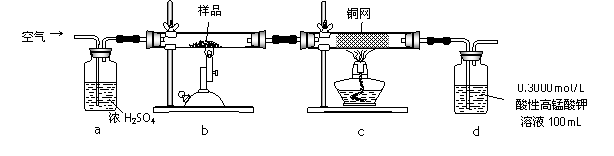
实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。
(已知:5SO2 + 2KMnO4 + 2H2O == K2SO4 + 2MnSO4 + 2H2SO4 )
请回答下列问题:
(1)称量样品质量能否用托盘天平_______(填“能”或“不能”),取出d中溶液10mL需要用______准确量取(填序号)
A.容量瓶 B.量筒 C.碱式滴定管 D.酸式滴定管
 (2)上述反应结束后,仍需通一段时间的空气,其目的是_______________________________
(2)上述反应结束后,仍需通一段时间的空气,其目的是_______________________________
(3)已知草酸与高锰酸钾酸性溶液作用有CO2和Mn2+等物质生成,则滴定时发生反应的离子方程式为_______________________________________﹔判断滴定到达终点的方法是_____________________________________________
(4)已知滴定管初读数为0.10mL,末读数如右图所示,消耗草酸溶液的体积为___________mL,
下列操作会导致该样品中FeS2的纯度测定结果偏高的是_________(填序号)
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(5)该样品中FeS2的纯度为__________________
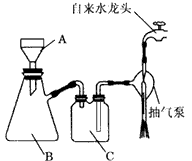
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是_______(填编号)
 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com