
题目列表(包括答案和解析)
某学校同学进行乙醇的化学性质实验探究学习,以下为他们的学习过程。
(一)结构分析
(1)写出乙醇的结构式 ;官能团的电子式 。
(二)性质预测
(2)对比乙醇和乙烷的结构,经过讨论,同学们认为乙醇分子中氧原子吸引电子能力较强,预测在一定条件下分子中 键(填写具体共价键)容易发生断裂。为此,他们查阅了相关资料,获得了以下乙醇性质的部分事实。
|
下列关于乙醇结构和性质的分析、理解错误的是
A.-OH对-C2H5的影响使乙醇与钠的反应比水与钠的反应速率慢ks5u
B. 乙醇在浓硫酸催化下,170℃时脱水生成乙烯的反应为消去反应
C. 乙醇的核磁共振氢谱图上有3个吸收峰,其强度之比为3︰2︰1,与钠反应的是
吸收强度最小的氢原子
 D. 乙醇与甲醚互为官能团异构体
D. 乙醇与甲醚互为官能团异构体
(三)设计方案、进行实验
甲同学用4mL 95%的乙醇、8mL90%浓硫酸、
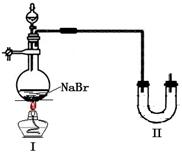
6g溴化钠研究乙醇转化为溴乙烷的反应。右图
是他设计的实验装置图(已省略部分夹持仪器)。
请回答有关问题。
(3)预计实验时装置Ⅰ主要发生两个反应,写出反应②的化学方程式。
![]() ①2NaBr + H2SO4 2HBr + Na2SO4,
①2NaBr + H2SO4 2HBr + Na2SO4,
②
(4)实验过程中,观察到反应后期烧瓶内液体颜色变棕黑,U形管右边与大气相通的导管口产生大量有刺激性气味的白雾,U形管内有少量淡黄色液体,该液体的有机成分是 。若要获得纯净的溴乙烷,方法是:实验结束后 。
(四)反思与改进
(5)乙同学认为:实验所用浓硫酸必须进行稀释,目的是 (填字母),稀释后的浓硫酸应放在 (填实验仪器名称)中。
A.减少HBr的挥发 B.防止浓硫酸分解产生SO2
C.减少副产物乙烯和乙醚的生成 D.减少Br2的生成
(6)丙同学提出应该对实验装置进行改进,请为两部分装置选择正确的措施:
A.不作改变 B.保留酒精灯加热,增加温度计且温度计水银球插入反应液中
C.水浴加热 D.冰水混合物冷却
装置Ⅰ ;装置Ⅱ 。请你再提出一条改进措施 。
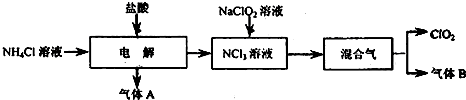

某研究性学习小组探究溴的制备及提纯
●资料收集
| 溴 | 物理性质 | 暗红色液体,刺激性气味。室温下易挥发。熔点-7.2℃,沸点59.1℃。密度2.928g?cm-3。稍溶于冷水。 |
| 化学性质 | 溶于水生成次溴酸 |
●溴的制备
现只有下列试剂:溴化钾、MnO2、浓盐酸、稀硫酸、浓硫酸
(1)写出制取溴的化学方程式: 。
现只有下列仪器:(石棉网、导管、铁架台、塞子等略去)

(2)根据反应原理,制备和收集溴应该选择的仪器有: (填字母序号)。
●溴的提纯
实验室用蒸馏法提纯液溴,装置如图所示。

(3)蒸馏装置都用磨口玻璃器具,而不用橡胶管和橡胶塞连接,是因为
。
(4)装置4的作用是 。
(5)要想除去液溴中少量Cl2,可在液溴中加入 (填序号)后再分液分离即可。
①48%的氢溴酸 ②浓NaOH溶液 ③饱和KI溶液
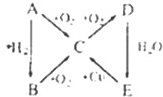 2009年7月21日,山东省某金矿发生硝酸泄露事故.由于浓硝酸易挥发且不稳定,事故发生时,有大量黄色、刺激性气味的烟雾产生.消防官兵到达后,立即对泄露硝酸进行处理(大量抛洒某种固体粉末等),及时地消除了事故带来的危害.
2009年7月21日,山东省某金矿发生硝酸泄露事故.由于浓硝酸易挥发且不稳定,事故发生时,有大量黄色、刺激性气味的烟雾产生.消防官兵到达后,立即对泄露硝酸进行处理(大量抛洒某种固体粉末等),及时地消除了事故带来的危害.
| ||
| ||
| ||
| △ |
| ||
| △ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com