
题目列表(包括答案和解析)
 常温下有浓度均为0.1mol?L-1的四种溶液:①碳酸钠溶液;②碳酸氢钠溶液;③盐酸;④氨水.请根据题目要求回答下列问题.
常温下有浓度均为0.1mol?L-1的四种溶液:①碳酸钠溶液;②碳酸氢钠溶液;③盐酸;④氨水.请根据题目要求回答下列问题.| c(OH-) | c(NH3?H2O) |
常温下有浓度均为0.1mol·L-1的四种溶液:①碳酸钠溶液;②碳酸氢钠溶液;③盐酸;④氨水。请根据题目要求回答下列问题。
(1) 上述溶液中,既能与氢氧化钠溶液反应,又能与硫酸溶液反应的是__________。
(2) 取适量溶液④,加入少量氯化铵固体,此时溶液中 ![]() 的值_____(填“增大” 或“减小”或“不变”)。
的值_____(填“增大” 或“减小”或“不变”)。
(3) 将等体积的③和④的溶液混合后,所得溶液中离子浓度由大到小的顺序是:__________。 所得溶液的pH<7,用离子方程式表示其原因________________;混合后的溶液中由水电 离
出的c(OH-)____0.1 mol/L NaOH溶液中由水电离出的c(OH-) (填“>”、“<”或“=”)。
(4) 取10mL溶液③,加水稀释到500mL,则该溶液中由水电离出c(H+)=________________。
(5) 若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子物质的量浓度由大到小的关系是__________。
(6) 有相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.CH3COONH4;C.(NH4)2SO4; D.NH4Cl, 按pH由大到小的顺序排列_______ _(填序号)
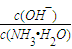 的值______(填“增大”或“减小”或“不变”).
的值______(填“增大”或“减小”或“不变”).
(10分)(1)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
①写出酸H2A的电离方程式__________________________。
②若溶液M由2 mol·L-1NaHA溶液与2mol·L-1NaOH溶液等体积混合而得,则溶液M的pH ____7 (填“>”、“<”或“=”);溶液M中各微粒的浓度关系正确的是 。
A.c(Na+)>c(A2-)>c(OH-)>c(H+)
B. c(HA-)+c(H2A) +c(H+)=c(OH-)
C.c(A2-)+c(HA-)+c(H2A)=1mol·L-1
D. c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+)
(2)室温时,氢氧化钙的溶度积KSP=4.7×10-6, 室温时将9 mL0.02 mol·L—1的氯化钙溶液与1 mL pH=13的氢氧化钠溶液混合后(溶液体积可直接加和),溶液中___ 沉淀析出(填“有”或“无”)。
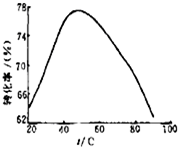
(3) 某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验:将固体加热,经测量剩余固体质量随时间变化如图所示。
则x:y= 。t2~t3时间段固体的化学式为 。t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色。则该时间所发生反应的化学方程式为 。
 蛇纹石可用于生产氢氧化镁,简要工艺流程如下:
蛇纹石可用于生产氢氧化镁,简要工艺流程如下:| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com