
题目列表(包括答案和解析)
 、Cl一四种离子,且c(
、Cl一四种离子,且c(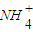 )>c(Cl-)>c(OH-)>c(H+),则这两种溶质是 .
)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是 .| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol H2、1mol I2 | 2 mol HI | 4 mol HI |
| HI的浓度 | C1 | C2 | C3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 反应物转化率 | a1 | a2 | a3 |
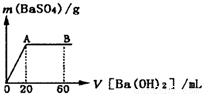
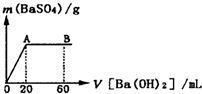 (2011?郑州二模)利用所学化学反应原理,解决以下问题:
(2011?郑州二模)利用所学化学反应原理,解决以下问题:| H | + 4 |
| H | + 4 |
 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol H2、1mol I2 | 2 mol HI | 4 mol HI |
| HI的浓度(mol?L-1) | C1 | C2 | C3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 反应物转化率 | a1 | a2 | a3 |
(2)取0.1mL 0.5mol×L-1的硫酸,稀释成100mL溶液,溶液的pH为________。
(3)0.1g氢氧化钠溶于蒸馏水配成50mL溶液,溶液的pH为________。
(4)pH=4的盐酸跟pH=10的氢氧化钡溶液等体积混合后,溶液的pH为________。
(5)pH为10和pH为12的氢氧化钠溶液,等体积混合后所得溶液的pH为________。
(6)NH3+H2OƒNH3×H2OƒNH4++OH-的平衡体系中,加入每种物质之后,下列各情况如何变化?
①溶解少量的氢氧化钠晶体后,平衡向________移动,溶液中c(OH-)________,pH________,电离程度________。
②溶解少量氯化氨晶体后,平衡向________移动,c(OH-)________,pH________,电离程度________。
③加入少量的醋酸后,平衡向________移动,c(OH-)________,pH________,电离程度________。
(1)25℃,纯水中c(H+)×c(OH-)=1´10-14;100℃时为1´10-12。温度升高,水的电离常数变________,水的离子积常数变________,这是由于水的电离是________热反应,100℃时,c(OH-)=1´10—6mol×L-1的溶液显________性。
(2)取0.1mL 0.5mol×L-1的硫酸,稀释成100mL溶液,溶液的pH为________。
(3)0.1g氢氧化钠溶于蒸馏水配成50mL溶液,溶液的pH为________。
(4)pH=4的盐酸跟pH=10的氢氧化钡溶液等体积混合后,溶液的pH为________。
(5)pH为10和pH为12的氢氧化钠溶液,等体积混合后所得溶液的pH为________。
(6)NH3+H2OƒNH3×H2OƒNH4++OH-的平衡体系中,加入每种物质之后,下列各情况如何变化?
①溶解少量的氢氧化钠晶体后,平衡向________移动,溶液中c(OH-)________,pH________,电离程度________。
②溶解少量氯化氨晶体后,平衡向________移动,c(OH-)________,pH________,电离程度________。
③加入少量的醋酸后,平衡向________移动,c(OH-)________,pH________,电离程度________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com