
题目列表(包括答案和解析)
 2011年6月,云南曲靖陆良化工实业有限公司5000多吨工业废料铬渣非法倾倒导致当地严重污染.+6价铬易被人体吸收,可致癌;+3价铬不易被人体吸收,毒性小.工业含铬废水的处理方法之一是将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的NaCl后进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.
2011年6月,云南曲靖陆良化工实业有限公司5000多吨工业废料铬渣非法倾倒导致当地严重污染.+6价铬易被人体吸收,可致癌;+3价铬不易被人体吸收,毒性小.工业含铬废水的处理方法之一是将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的NaCl后进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.(6分)2011年6月,云南曲靖陆良化工实业有限公司5000多吨工业废料铬渣非法倾倒导致当地严重污染。+6价铬易被人体吸收,可致癌;+3价铬不易被人体吸收,毒性小。工业含铬废水的处理方法之一是将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的NaCl后进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(已知:常温下Ksp Fe(OH)3=2.6×10-39,Ksp Cr(OH)3=6.0×10-31)
(1)若阳极铁质量减少16.8g,则理论上被还原的Cr2O72-的物质的量为 mol。
(2)已知电解后的溶液中c(Fe3+)为2.6×10-13 mol·L-1,则溶液中Cr3+浓度为 mol·L-1。
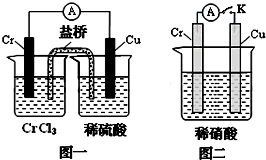
(3)在下图装置中,观察到图一装置铜电极上产生大量的无色气泡,而在图二装置中当开关K断开时,铬电极无现象,K闭合时,铬电极上产生大量无色气体,并变成红棕色气体。根据上述现象试推测金属铬的两个重要化学性质 、 。
(16分).铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。
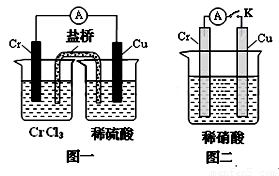
(1)在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图 2装置中铜电极上无气体产生,铬电极上产生大量有色气体。由图 1 知金属铬的活动性比铜_____(填强,弱),图 2装置中铬电极的电极反应式
(2)CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸, CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为_____________________________________________________________。
(3)存在平衡:2CrO42—(黄色)+2H+Cr2O72—(橙色)+H2O
①若平衡体系的pH=2,则溶液显 色.
②能说明第①步反应达平衡状态的是 。
a.Cr2O72—和CrO42—的浓度相同 b.2v (Cr2O72—) =v (CrO42—) c.溶液的颜色不变
(4)CrO3和K2Cr2O7均易溶于水,这是工业上造成铬污染的主要原因。净化处理方法之一是将含+6价 Cr 的废水放入电解槽内,用铁作阳极,加入适量的NaCl进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成 Fe(OH)3 和Cr(OH)3沉淀除去[已知 KspFe(OH)3=4.0×10-38,KspCr(OH)3=6.0×10-31]。
①电解过程中 NaCl 的作用是__________________________。
②已知电解后的溶液中c(Fe3+)为2.0×10-13 mol·L1,则溶液中c(Cr3+)为____ mol·L-1。
(5)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如下图所示。
从开始加热到 750K 时总反应方程式为_______________________。
(本题共16分)铁氧体是一类磁性材料,通式为MO·xFe2O3(M为二价金属离子),如Fe3O4可表示为FeO·Fe2O3,制备流程为:
根据题意回答:
1.现称取2.8 g铁粉,加入一定量的稀硫酸使其完全溶解后,再加入 g的FeCl3固体,经上述反应后,方可得到纯净的Fe3O4。
2.如果以MgSO4和FeCl3为原料,要获得18.0克MgO·2Fe2O3,在制取过程中至少需要1 mol/L的NaOH溶液 mL。
3.在一次制备Fe3O4的实验中,由于反应物比例控制不当,获得了另一种产品。取一定量该产品溶于足量盐酸中,还需通入标准状况下672 mLCl2才能把溶液中的Fe2+全部氧化为Fe3+,然后把所得溶液蒸干,灼烧至恒重,得9.6 g固体。该产品的化学式为 。
4.有一种在电子工业上应用广泛的含铬铁氧体,其组成可表示为: ,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为 。
,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为 。
(6分)2011年6月,云南曲靖陆良化工实业有限公司5000多吨工业废料铬渣非法倾倒导致当地严重污染。+6价铬易被人体吸收,可致癌;+3价铬不易被人体吸收,毒性小。工业含铬废水的处理方法之一是将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的NaCl后进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(已知:常温下Ksp Fe(OH)3=2.6×10-39,Ksp Cr(OH)3=6.0×10-31)
(1)若阳极铁质量减少16.8g,则理论上被还原的Cr2O72-的物质的量为 mol。
(2)已知电解后的溶液中c(Fe3+)为2.6×10-13 mol·L-1,则溶液中Cr3+浓度为 mol·L-1。
(3)在下图装置中,观察到图一装置铜电极上产生大量的无色气泡,而在图二装置中当开关K断开时,铬电极无现象,K闭合时,铬电极上产生大量无色气体,并变成红棕色气体。根据上述现象试推测金属铬的两个重要化学性质 、 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com