
题目列表(包括答案和解析)
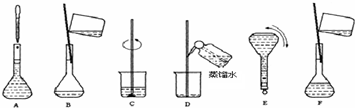
实验室配制500mL0.5 mol·L-1的NaOH溶液,有如下操作步骤:① 把称量好的NaOH固体放入小烧杯中,加适量蒸馏水溶解;② 把所得的溶液小心转入 A 中;③ 继续向容量瓶中加蒸馏水至液面距刻度标线2—3cm处,改用 B 小心滴加蒸馏水至溶液凹液面最低点与刻度标线
相切;④ 用少量蒸馏水洗涤烧杯和玻璃棒2—3次,每次洗涤的液体都要小心转入容量瓶,
并轻轻摇匀;⑤将容量瓶塞紧,充分摇匀;⑥ 充分搅拌,静置冷却。
(1)操作步骤正确的顺序为(填序号)____________________。
(2)上段文字中的A.B处相应的仪器应该是 和 ,该实验
用到的基本仪器还有玻璃棒、烧杯、__________________________________。
(3)若最终定容时俯视,则所配溶液的物质的量浓度比要求配制的浓度(填“偏高”、
“偏低”、或“无影响”,下同)____________。
(4)若没有进行操作④,则所配溶液的浓度会________, 若加蒸馏水不慎超过了刻度
标线,浓度会___________。
实验室配制500mL0.5 mol·L-1的NaCl溶液,有如下操作步骤:① 把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解;② 把①所得的溶液小心转入 A 中;③ 继续向容量瓶中加蒸馏水至液面距刻度标线2—3cm处,改用 B 小心滴加蒸馏水至溶液凹液面最低点与刻度标线相切;④ 用少量蒸馏水洗涤烧杯和玻璃棒2—3次,每次洗涤的液体都要小心转入容量瓶,并轻轻摇匀;⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序为(填序号)____________________。
(2)上段文字中的A.B处相应的仪器应该是______ 和______,该实验用到的基本仪器还有________________________________________。
(3)若最终定容时俯视,则所配溶液的物质的量浓度比要求配制的浓度(填“偏高”、“偏低”、或“无影响”,下同)____________。
(4)若没有进行操作④,则所配溶液的浓度会________, 若加蒸馏水不慎超过了刻度标线,浓度会___________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com