(2013?北京一模)人类的生产和生活都离不开金属.
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是
Al
Al
.金属以矿物形式存在,下列矿石的主要成分属于氧化物的是
Fe2O3、Al2O3
Fe2O3、Al2O3
(填化学式).
赤铁矿 孔雀石 铝土矿
(主要成分Fe
2O
3)〔主要成分Cu
2(OH)
2CO
3〕(主要成分Al
2O
3)
(2)金属的回收和利用是保护金属资源的一种有效途径.
①废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为
.
②向含有AgNO
3、Cu(NO
3)
2、Zn(NO
3)
2的混合溶液中加入一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是
C
C
A.固体中一定有Fe、Ag,可能有 Cu、Zn
B. 固体中一定有Fe、Zn,可能有 Cu、Ag
C.滤液中一定含Fe
2+、Zn
2+,不含Cu
2+、Ag
+D.滤液中一定含Zn
2+、Fe
2+,可能含Cu
2+(3)某次实验结束时,同学们将含有CuSO
4、ZnSO
4、FeSO
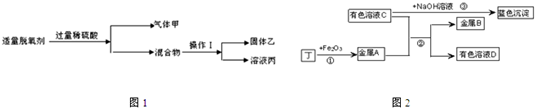
4的废液倒在废液缸里,如果将废液直接排放会造成水污染.于是几位同学利用课余时间处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下:

请回答:
①操作1的名称是
过滤
过滤
;固体A的成分为
Zn、Fe、Cu
Zn、Fe、Cu
.
②若要检验向固体C中加入的稀硫酸是否足量的方法是
取少量铜,加适量稀硫酸,若无气泡产生,证明硫酸足量
取少量铜,加适量稀硫酸,若无气泡产生,证明硫酸足量
.
③若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量废液的质量、蒸发得到固体硫酸锌的质量和
操作1中加入锌粉的质量
操作1中加入锌粉的质量
..


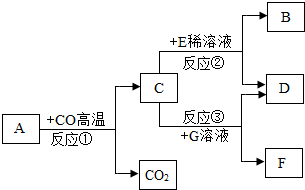 (2012?日照)现有A~G七种物质,已知A是赤铁矿的主要成分,E的浓溶液稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系:
(2012?日照)现有A~G七种物质,已知A是赤铁矿的主要成分,E的浓溶液稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系: